

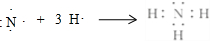 ,
,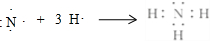 ;
;

科目:高中化学 来源: 题型:
A、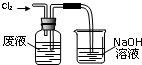 氧化废液中的溴化氢 |
B、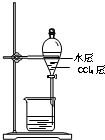 分离CCl4层和水层 |
C、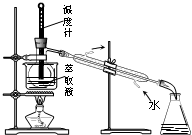 分离CCl4和液溴 |
D、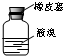 用仪器丁长期贮存液溴 |
查看答案和解析>>
科目:高中化学 来源: 题型:
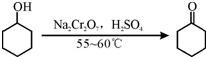 其反应的装置示意图如图1(夹持装置、加热装置略去):
其反应的装置示意图如图1(夹持装置、加热装置略去):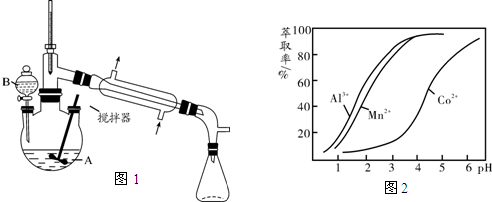
| 物质 | 沸点(℃) | 密度(g?cm-3,20℃) | 溶解性 |
| 环己醇 | 161.1(97.8) | 0.9624 | 能溶于水 |
| 环己酮 | 155.6(95) | 0.9478 | 微溶于水 |
| 饱和食盐水 | 108.0 | 1.3301 | |
| 水 | 100.0 | 0.9982 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、绚丽缤纷的烟花中添加了含钾、钠、钙、铜等金属元素的化合物 |
| B、为防止中秋月饼等富脂食品氧化变质,常在包装袋中放入生石灰 |
| C、停车场安装催化光反应设施,可使汽车尾气中的CO和NOX反应生成无毒气体 |
| D、氮化硅陶瓷、氧化铝陶瓷、光导纤维等属于新型无机非金属材料 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、SiO2和A12O3都既能与酸反应,又能与碱反应 |
| B、硫化钠溶于水中发生反应的离子方程式为S2-+2H2O?H2S+2OH- |
| C、3.2 g Cu与5.5 mL l8.4 mol?L -1的浓H2SO4充分反应,转移的电子数为6.02×1022 |
| D、由水电离的c(H+)=1×10 -13mol?L -1的溶液中Cl-、HCO3-、NO3-、NH4+能大量共存 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 放电 |
| 充电 |
| A、放电时负极反应为:Zn-2e-+2OH-=Zn(OH)2 |
| B、充电时阳极反应为:Fe(OH)3-3e-+5OH-=FeO42-+4H2O |
| C、放电时每转移3mol电子,正极有1molK2FeO4被氧化 |
| D、放电时的正极在充电时须接电源正极 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com