
| A. | 2 mol•L-1 | B. | 4 mol•L-1 | C. | 6 mol•L-1 | D. | 8 mol•L-1 |
分析 该过程中发生的反应为:Fe3O4+8HCl=2FeCl3+FeCl2+4H2O、Fe+2HCl=FeCl2+H2↑、2FeCl3+Fe=3FeCl2、FeCl2+2NaOH=Fe(OH)2↓+2NaCl、NaOH+HCl=NaCl+H2O,最终溶液中的溶质是NaCl,根据原子守恒计算盐酸的浓度.
解答 解:该过程中发生的反应为:Fe3O4+8HCl=2FeCl3+FeCl2+4H2O、Fe+2HCl=FeCl2+H2↑、2FeCl3+Fe=3FeCl2、FeCl2+2NaOH=Fe(OH)2↓+2NaCl、NaOH+HCl=NaCl+H2O,最终溶液中的溶质是NaCl,原子守恒得n(NaOH)=n(NaCl)=n(HCl),则c(HCl)=$\frac{n(NaOH)}{V(HCl)}$=$\frac{5mol/L×0.16L}{0.1L}$=8 mol•L-1,
故选D.
点评 本题考查了方程式的计算,明确最终溶液中的溶质是解此题关键,再结合原子守恒解答即可,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 氢气和氯气光照爆炸得到HCl气体 | |
| B. | 在HCl合成塔,点燃的氢气中通入氯气产生HCl | |
| C. | 氯气在空气中点燃后通入氢气产生HCl | |
| D. | 点燃氢气和氯气混合气体产生HCl气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
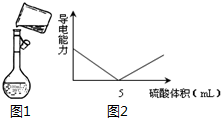 用98%的浓硫酸(密度为1.84g/mL)配制500mL 0.30mol/L 稀硫酸的实验步骤如下:①计算所用浓硫酸的体积;②量取一定体积的浓硫酸;③稀释;④冷却,转移、洗涤摇匀;⑤定容、摇匀;⑥转入试剂瓶,贴标签.
用98%的浓硫酸(密度为1.84g/mL)配制500mL 0.30mol/L 稀硫酸的实验步骤如下:①计算所用浓硫酸的体积;②量取一定体积的浓硫酸;③稀释;④冷却,转移、洗涤摇匀;⑤定容、摇匀;⑥转入试剂瓶,贴标签.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 取少量溶液滴加Ca(OH)2溶液,观察是否出现白色浑浊,确定NaHCO3溶液中是否混有Na2CO3 | |
| B. | 苯酚沾到皮肤上,先用酒精清洗,再用水冲洗 | |
| C. | 将10g ZnSO4•7H2O溶解在90g水中,配制10%ZnSO4溶液 | |
| D. | 向稀硫酸中加几滴CuSO4溶液,可提高纯锌与稀硫酸的反应速率. |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 生成白色沉淀、有气体产生 | B. | 生成红褐色沉淀、有气体产生 | ||
| C. | 生成红褐色沉淀 | D. | 生成黑色沉淀、有气体产生 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HSO3-在溶液中发生水解:HSO3-+H2O?SO32-+H3O+ | |
| B. | 向Mg(OH)2浊液中滴加FeCl3溶液生成红褐色沉淀:3OH-+Fe3+=Fe(OH)3↓ | |
| C. | 碳酸氢钠溶液显碱性:HCO3-+H2O?H2CO3+OH- | |
| D. | 惰性电极电解MgCl2溶液:Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$OH-+Cl2↑+H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.75 mol/L | B. | 1.5 mol/L | C. | 0.25 mol/L | D. | 0.5 mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
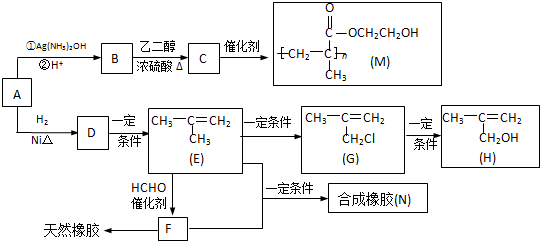
 ;
; .
.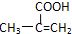 ,该不饱和酸有多种同分异构体,属于酯类且含有碳碳双键的同分异构体共有5种.
,该不饱和酸有多种同分异构体,属于酯类且含有碳碳双键的同分异构体共有5种.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1molBr2+2molHBr | B. | 3molHBr | C. | 4molBr2+2molH2 | D. | 2molHBr |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com