
【题目】如图所示晶体结构是一种具有优良的电压、电光等功能的晶体材料的最小结构单元(晶胞).晶体内与每个“Ti”紧邻的氧原子数和这种晶体材料的化学式分别是(各元素所带电荷均已略去)( )
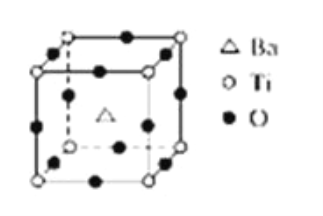
A. 8;BaTi8O12
B. 8;BaTi4O9
C. 6;BaTiO3
D. 3;BaTi2O3
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A. 所有铵盐受热均可以分解,产物均有NH3
B. 所有铵盐都易溶于水,所有铵盐中的N均呈-3价
C. NH4Cl溶液中加入NaOH浓溶液共热时反应的离子方程式为NH4++OH-![]() NH3↑+H2O
NH3↑+H2O
D. NH4Cl和NaCl的固体混合物可用升华法分离
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有14.4gCO和CO2的混合气体,在标准状况下其体积为8.96L。
(1)将混合气体依次通过下列如图所示装置,最后收集在气球中(实验在标准状况下测定)。

①气球中收集到的气体的摩尔质量为___。
②收集到气球中的气体的电子总数为____(用NA表示阿伏加德罗常数的值)。
(2)求该混合气体的平均摩尔质量(要有计算过程)___
(3)求混合气体中碳原子的个数(用NA表示阿伏加德罗常数的值,且要有计算过程)。___
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是
A. NO2、BF3、NCl3分子中没有一个分子中原子的最外层电子都满足了8电子稳定结构
B. P4和CH4都是正四面体型分子且键角都为109.5°
C. NH4+的电子式为 ,离子呈平面正方形结构
,离子呈平面正方形结构
D. NH3分子中有一对未成键的孤电子对,它对成键电子的排斥作用较强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关有机化合物的说法正确的是
A. 麦芽糖的水解产物有两种,且互为同分异构体
B. 等质量的苯和苯乙烯完全燃烧,消耗氧气的体积在相同条件下不相同
C. 间二甲苯中苯环上的一个氢原子被“![]() ”取代时,有9种结构(不考虑立体异构)
”取代时,有9种结构(不考虑立体异构)
D. ![]() 与甲苯或甘油在一定条件下发生反应,其反应类型不同
与甲苯或甘油在一定条件下发生反应,其反应类型不同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】ⅡBⅥA族半导体纳米材料(如CdTe、CdSe、ZnSe、ZnS等)在光电子器件、太阳能电池以及生物探针等方面有广阔的前景。回答下列问题:
(1)基态锌(Zn)原子的电子排布式为[Ar]_____。
(2)“各能级最多容纳的电子数,是该能级原子轨道数的二倍”,支撑这一结论的理论是______(填标号)
a 构造原理 b 泡利原理 c 洪特规则 d 能量最低原理
(3)在周期表中,Se与As、Br同周期相邻,与S、Te同主族相邻。Te、As、Se、Br的第一电离能由大到小排序为_______。
(4)H2O2和H2S的相对分子质量相等,常温下,H2O2呈液态,而H2S呈气态,其主要原因是______;![]() 的中心原子杂化类型为_______,其空间构型为_______。
的中心原子杂化类型为_______,其空间构型为_______。
(5)ZnO具有独特的电学及光学特性,是一种应用广泛的功能材料。
①已知锌元素、氧元素的电负性分别为1.65、3.5,ZnO中化学键的类型为______。ZnO可以被NaOH溶液溶解生成[Zn(OH)4]2—,请从化学键角度解释能够形成该离子的原因。_______。

②一种ZnO晶体的晶胞如图所示。晶胞边长为a nm、阿伏加德罗常数的值为NA,其晶体密度为________g·cm3。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下联氨(![]() )的水溶液中有:① N2H4+H2O
)的水溶液中有:① N2H4+H2O![]() N2H5++OH- K1
N2H5++OH- K1
② N2H5++H2O![]() N2H62++OH- K2,该溶液中微粒的物质的量分数
N2H62++OH- K2,该溶液中微粒的物质的量分数![]() 随
随![]() 变化的关系如图所示。下列叙述错误的是
变化的关系如图所示。下列叙述错误的是

A. 图中Ⅲ对应的液粒为![]()
B. 由图可知,![]()
C. 若![]() 点为
点为![]() 溶液,则存在:
溶液,则存在:![]()
D. 反应②为![]() 的水解方程式
的水解方程式
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于在一定条件下的密闭容器中进行的反应:A(g)+3B(g)![]() 2C(g).下列说法正确的是
2C(g).下列说法正确的是
A. 压缩使容器体积减小,逆反应速率增大
B. 在等温等压条件下,若体系密度不变,则反应不一定平衡
C. 物质A的浓度增大,会减慢反应速率
D. 在高温,高压和有催化剂的条件下,A与B能100%转化为C
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知胆矾溶于水时溶液温度降低,胆矾分解的热化学方程式为:CuSO45H2O(s)=CuSO4(s)+5H2O(l) ΔH=+Q1kJ·mol-1;室温下,若将1 mol无水硫酸铜溶解为溶液时放热Q2kJ,则()
A. Q1>Q2 B. Q1=Q2 C. Q1<Q2 D. 无法比较
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com