
【题目】如图是实验室制取SO2并验证SO2的某些性质的装置,试回答
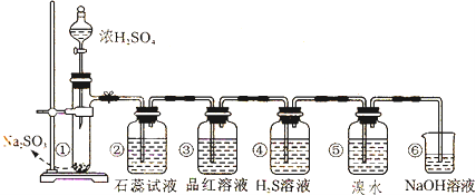
试回答:
(1)①中发生反应的化学方程式为____________________________.
(2)②中的实验现象为____________,此实验说明SO2是_______氧化物.
(3)③的品红溶液______________,证明SO2有_____________性.
(4)④中的实验现象为______________,此实验说明SO2有____________性.
(5)⑤中的实验现象为____________,此实验说明SO2有________性.
(6)⑥的作用是___________,反应方程式是__________________________
【答案】 Na2SO3+H2SO4(浓)=Na2SO4+SO2↑+H2O 溶液变红 酸性 溶液褪色 漂白 产生黄色沉淀 氧化 溶液褪色 还原 尾气处理 SO2+2NaOH=Na2SO3+H2O
【解析】(1)①中为亚硫酸钠和浓硫酸反应生成二氧化硫气体,反应的化学方程式为:Na2SO3+H2SO4(浓)=Na2SO4+SO2↑+H2O;
(2)氧化硫溶于水和水反应生成亚硫酸,亚硫酸为弱酸,可以使紫色石蕊试液变红,故答案为:溶液变红;酸性;
(3)二氧化硫与品红化合生成无色物质,能使品红溶液褪色,故二氧化硫具有漂白性,故答案为:溶液褪色;漂白性;
(4)SO2中+4价S具有氧化性,硫化氢中2价S具有还原性,二氧化硫能把硫化氢氧化成单质硫,发生归中反应,反应方程式为SO2+2H2S=3S↓+2H20,生成的S是黄色沉淀,故答案为:产生淡黄色沉淀;氧化;
(5)二氧化硫具有还原性,能够与溴水发生氧化还原反应生成氢溴酸和硫酸,溴水褪色,故答案为:溶液褪色;还原;
(6)二氧化硫有毒,不能直接排放到空气中,二氧化硫酸性氧化物能够与氢氧化钠反应生成亚硫酸钠和水,所以可以用氢氧化钠溶液吸收二氧化硫,反应的化学方程式为:2NaOH+SO2=Na2SO3+H2O;故答案为:吸收尾气;SO2+2NaOH=Na2SO3+H2O.


 世纪百通主体课堂小学课时同步达标系列答案
世纪百通主体课堂小学课时同步达标系列答案 世纪百通优练测系列答案
世纪百通优练测系列答案 百分学生作业本题练王系列答案
百分学生作业本题练王系列答案科目:高中化学 来源: 题型:
【题目】分类是科学研究的重要方法,下列物质分类正确的是
A. 强酸:盐酸、醋酸 B. 电解质:H2SO4、NaOH
C. 胶体:豆浆、氯化铁溶液 D. 氧化剂:Mg,KMnO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锂锰电池的体积小,性能优良,是常用的一次电池.该电池反应原理如图所示,其中电解质LiClO4溶于混合有机溶剂中,Li+ 通过电解质可以自由迁移,正极反应式为:MnO2+Li++e﹣=LiMnO2 . 回答下列问题:
(1)外电路的电子方向是由极流向极.(填字母)
(2)该电池的负极反应式为 .
(3)如果14g的锂完全溶解放电,所产生的电量用来电解水,会产生L的H2(在标准状况下).
(4)MnO2可与KOH和KClO3在高温条件下反应,生成K2MnO4 , 反应的化学方程式为 , K2MnO4在酸性溶液中歧化,生成KMnO4和MnO2的物质的量之比为 . 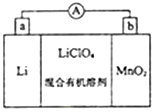
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】质量数是 37 的原子, 可能有( )
A.19 个质子, 18 个中子, 20 个电子
B.18 个质子, 19 个中子, 18 个电子
C.19 个质子, 18 个中子, 18 个电子
D.17个质子, 20 个中子, 18 个电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子的检验能达到预期目的是( )
A. 检验![]() :先滴加氯水,再滴加KSCN溶液,若变红,则有Fe2+
:先滴加氯水,再滴加KSCN溶液,若变红,则有Fe2+
B. 检验NH4+:先滴加NaOH溶液,加热,用湿润蓝色石蕊试纸检验,若变红,则有NH4+
C. 检验Cl—:先滴加AgNO3溶液,再滴加硝酸,若有白色沉淀,则有Cl—
D. 检验![]() :滴加硝酸,将生成的气体通入品红溶液,若品红溶液褪色,则有
:滴加硝酸,将生成的气体通入品红溶液,若品红溶液褪色,则有![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜及其化合物在生产、生活中有广泛的应用.
(1)铜可采用如下方法制备:火法炼铜:Cu2S+O2 ![]() 2Cu+SO2
2Cu+SO2
湿法炼铜:CuSO4+Fe═FeSO4+Cu
上述两种方法中,铜元素均被(填“氧化”或“还原”)成铜单质.
(2)印刷电路板上使用的铜需要回收利用.方法一:用FeCl3溶液浸泡印刷电路板制备CuCl22H2O,实验室模拟回收过程如下:![]()
①证明步骤Ⅰ所加FeCl3溶液过量的方法是 .
②步骤2中所加的氧化剂最适宜的是 .
A.HNO3B.H2O2C.KMnO4
③步骤3的目的是使溶液的pH升高到4.2,此时Fe3+完全沉淀,可选用的“试剂1”是 . (写出一种即可)
④蒸发农缩CuCl2溶液时,要滴加浓盐酸,目的是(用化学方程式并结合简要的文字说明),再经冷却、结晶、过滤,得到CuCl22H2O.
方法二:用H2O2和稀硫酸共同浸泡印刷电路板制备硫酸铜时,其热化学方程式是:
Cu(s)+H2O2(l)+H2SO4(nq)═CuSO4(aq)+2H2O(l)△H1=﹣320kJ/mol
又知:2H2O(l)═2H2O(l)+O2(g)△H2=﹣196kJ/mol
H2(g)+ ![]() O2(g)═H2O(l)△H3=﹣286kJ/mol
O2(g)═H2O(l)△H3=﹣286kJ/mol
则反应Cu(s)+H2SO4(aq)═CuSO4(aq)+H2(g)的△H= .
(3)欲实现反应Cu+H2SO2═CuSO4+H2 , 在你认为能实现该转化的装置中的括号内,标出电极材料(填“Cu”或“C”)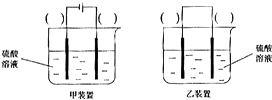
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化铁溶液与氢氧化铁胶体具有的共同性质是( )
A. 分散质粒子直径在1~100 nm之间B. 都是混合物
C. 都是无色、透明的溶液D. 都呈红褐色
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com