
 己知H2O2的分子空间结构如图,两个平面的夹角为93°,两个O-H键与O-O键之间的夹角均为96°.有关H2O2结构的说法中不正确的是( )
己知H2O2的分子空间结构如图,两个平面的夹角为93°,两个O-H键与O-O键之间的夹角均为96°.有关H2O2结构的说法中不正确的是( )| A. | 过氧化氢分子中氧原子sp3杂化 | B. | 易溶于有机溶剂 | ||
| C. | 过氧化氢分子间存在氢键 | D. | H2O2是极性分子 |
分析 A.由H2O2的结构可知,O原子形成1个O-H键、1个O-O键,含有2对孤对电子,杂化轨道数为4;
B.根据相似相溶原理分析判断;
C.O的电负性较大,易形成氢键;
D.H2O2分子中,O-O键非极性键,而O-H键为极性键,结构不对称.
解答 解:A.由H2O2的结构可知,O原子形成1个O-H键、1个O-O键,含有2对孤对电子,杂化轨道数为4,杂化方式为sp3,故A正确;
B.H2O2分子中,O-O键非极性键,而O-H键为极性键,结构不对称,正负电荷重心不重合,为极性分子,易溶于极性溶剂,难溶于非极性的有机溶剂,故B错误;
C.O的电负性较大,易形成氢键,所以过氧化氢分子间存在氢键,故C正确;
D.H2O2分子中,O-O键非极性键,而O-H键为极性键,结构不对称,正负电荷重心不重合,为极性分子,故D正确.
故选B.
点评 本题考查了双氧水的结构和性质,侧重于共价键的考查,注意把握双氧水中键的极性和分子的极性,难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:解答题

 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将Cl2与HCl混合气体通过饱和食盐水可得到纯净的Cl2 | |
| B. | 向FeCl2溶液中滴加氯水,溶液颜色变成棕黄色,说明氯水中含有HClO | |
| C. | SiO2既能和氢氧化钠溶液反应也能和氢氟酸反应,所以是两性氧化物 | |
| D. | 将浓硫酸滴到蔗糖表面,固体变黑膨胀,说明浓硫酸有脱水性和强氧化性 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| pH | 1.3 | 1.4 | 1.5 | 1.6 | 1.7 | 1.8 | 1.9 | 2.0 | 2.1 |
| 钒沉淀率/% | 88.1 | 91.8 | 96.5 | 98 | 99.8 | 9.8 | 96.4 | 93.0 | 89.3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向某溶液中滴加BaCl2溶液,若有白色沉淀,再滴加足量稀HNO3,若沉淀不溶解,则说明原溶液中一定含SO42- | |
| B. | 向某溶液中先滴加硝酸再滴加KSCN溶液,若溶液出现血红色则说明原溶液中含Fe3+ | |
| C. | 向某溶液中滴加足量稀HCl,产生的气体能使澄清石灰水变浑浊,则说明原溶液中一定含CO32-或HCO3- | |
| D. | 向某盐溶液中滴加NaOH溶液并加热,产生使湿润的红色石蕊试纸变蓝的气体,则原溶液含NH4+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
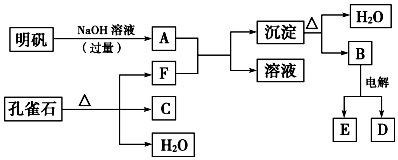
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 离子 | 开始沉淀的PH | 沉淀完全的PH |
| Cr3+ | 4.9 | 6.8 |
| Fe3+ | 1.5 | 4.1 |
| 物质 | 溶解度/(g/110g水) | ||
| 0℃ | 40℃ | 80℃ | |
| K2SO4 | 7.4 | 14.8 | 21.4 |
| K2Cr2O7 | 4.7 | 26.3 | 73 |
| 实验序号 | 待测样品溶液的体积/mL | 0.1000mol/L摩尔盐溶液的体积/mL | |
| 滴定前刻度 | 滴定后刻度 | ||
| 1 | 25.00 | 0.00 | 24.98 |
| 2 | 25.00 | 1.56 | 29.30 |
| 3 | 25.00 | 1.00 | 26.02 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 Ⅰ.铅的冶炼有很多种方法.
Ⅰ.铅的冶炼有很多种方法.| 温度/℃ | 300 | 727 | 1227 |
| 1gK | 6.17 | 2.87 | 1.24 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com