
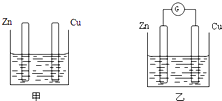
 �ֱ�ͼ�мס�����ʾװ�ý���ʵ�飬ͼ�������ձ������ҺΪͬŨ�ȵ�ϡ���ᣬ����GΪ�����ƣ���ش��������⣺
�ֱ�ͼ�мס�����ʾװ�ý���ʵ�飬ͼ�������ձ������ҺΪͬŨ�ȵ�ϡ���ᣬ����GΪ�����ƣ���ش��������⣺


| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
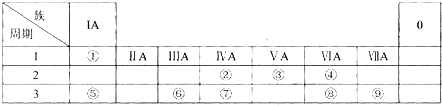
| A��ԭ�Ӱ뾶A��B��C |
| B������B��һ�������¿���ͨ���û���Ӧ�õ�����A |
| C��C����������۵��A��������ĵ� |
| D��A��C���γ����ӻ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ||

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 2010�괺�������ڵᡢǭ�����塢����ʡ�����غ���ǣ����ȫ��������ģ�ˮ��������������Ҫ��ѧ���ʣ��й�ˮ�ķ�Ӧ�к࣮ܶ
2010�괺�������ڵᡢǭ�����塢����ʡ�����غ���ǣ����ȫ��������ģ�ˮ��������������Ҫ��ѧ���ʣ��й�ˮ�ķ�Ӧ�к࣮ܶ
| ||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����״̬�£�3.4g NH3�к�N-H����ĿΪ0.2N |
| B���ö��Ե缫��ⱥ��ʳ��ˮ��ÿ����22.4L H2ת�Ƶ�����Ϊ2NA |
| C�������£�5.6g��ϩ�ͻ�����Ļ�������к��е�̼ԭ����Ϊ0.4NA |
| D�����ܱ������м���2mol SO2��1mol O2����ַ�ӳ��ɵ�2NA��SO2���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��ˮ�����ӻ����� |
| B���ܶȻ����� |
| C������٤������ |
| D������ĵ���ƽ�ⳣ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A������Һ��c��H2SO3����c��SO32-�� |
| B������Һ��ˮ����̶ȱȴ�ˮ�еĴ� |
| C������Һ��c��Na+��+c��H+��=c��SO32-��+c��HSO3-��+c��OH-�� |
| D������Һ��c��SO32-��+c��HSO3-��+c��H2SO3��=0.08mol?L-1 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com