
| A. | 150mL 1mol•L-1的NaCl | B. | 25mL 2mol•L-1的FeCl3 | ||
| C. | 150mL 3mol•L-1的KCl | D. | 75mL 2mol•L-1的CaCl2 |
分析 50mL1mol/L的AlCl3溶液中的Cl-浓度为3mol/L,根据溶质化学式计算各选项中的Cl-物质的量,进行比较可知.注意溶液中溶质离子的浓度与溶液体积无关,只取决于物质电离出的离子的数目多少与溶质的浓度.
解答 解:50mL1mol/L的AlCl3溶液中的Cl-浓度为3mol/L.
A.150 mL 1 mol•L-1的NaCl溶液中Cl-浓度为1mol/L,故A错误;
B.25 mL 2 mol•L-1的FeCl3溶液中Cl-浓度为2mol/L×3=6mol/L,故B错误;
C.150 mL 3 mol•L-1的KCl溶液中Cl-浓度为3mol/L,故C正确;
D.75 mL 2 mol•L-1的CaCl2溶液中Cl-浓度为2mol/L,故D错误.
故选C.
点评 本题考查了物质的量浓度的计算,题目难度不大,试题侧重基础知识的考查,注意掌握物质的量浓度的概念及计算方法,明确物质的量浓度与溶液体积大小无关.


科目:高中化学 来源: 题型:选择题
| A. | 雾是溶液,能永久在空气中稳定存在 | |
| B. | 雾的胶体,一段时间内能稳定存在 | |
| C. | 雾是乳浊液,不能稳定存在 | |
| D. | 雾的悬浊液,在空气中能沉降 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 16g O2中含有的氧分子数为NA | |
| B. | 1mol Zn变为Zn2+时失去的电子数目为NA | |
| C. | 常温常压下,11.2 L H2中含有的氢分子数为0.5NA | |
| D. | 1L 1 mol•L-1 BaCl2溶液中含有的钡离子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CaCO3→CO2 | B. | HClO→O2 | C. | HCl(浓)→MnCl2 | D. | NaBr→NaCl |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 化学键 | C-C | C-H | H-H | C-O | C≡O | H-O |
| 键能/kJ•mol-1 | 348 | 413 | 436 | 358 | 1072 | 463 |
| 反应时间/min | 0 | 5 | 10 | 15 | 20 | 25 |
| 压强/MPa | 12.6 | 10.8 | 9.5 | 8.7 | 8.4 | 8.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 使用催化剂可加快SO2转化为SO3的速率 | |
| B. | H2、I2、HI平衡混合气加压后颜色变深 | |
| C. | 装有NO2、N2O4平衡混合气的玻璃球在冷水中气体颜色变浅 | |
| D. | SO2通入氯水,氯水的颜色变浅 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
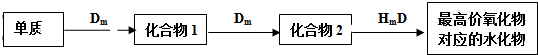
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com