
分析 2Al+6HCl═2AlCl3+3H2↑中,H元素的化合价降低被还原,则HCl为氧化剂,Al元素的化合价升高被氧化,则Al为还原剂,该反应中转移6e-;
解答 解:H元素的化合价由+1降低为0,Al元素的化合价由0升高为+3价,则HCl为氧化剂,H元素被还原,Al为还原剂,Al元素被氧化,该反应中2molAl参加反应,转移6mol电子,则双线桥表示该反应电子转移的方向和数目为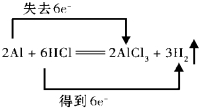 ,则氧化还原反应的实质是反应过程中有电子转移,常见的氧化还原反应为CuO+H2$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O,故答案为:
,则氧化还原反应的实质是反应过程中有电子转移,常见的氧化还原反应为CuO+H2$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O,故答案为: ;Al;HCl;Al;反应过程中有电子转移;CuO+H2$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O.
;Al;HCl;Al;反应过程中有电子转移;CuO+H2$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O.
点评 本题考查氧化还原反应,为高频考点,把握电子守恒、原子守恒及反应中元素化合价变化为解答的关键,侧重基本概念及转移电子的考查,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 烧碱溶液盛装在带有玻璃塞的试剂瓶中 | |
| B. | 少量金属钠保存在煤油中 | |
| C. | 向紫色石蕊试液中加入新制氯水,石蕊试液先变红后褪色 | |
| D. | 区别溶液和胶体的最简单的方法是丁达尔效应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
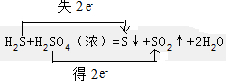 .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO32-、Cl- | B. | Na+、Cu2+ | C. | Mg2+、C1- | D. | C1-、Ba2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
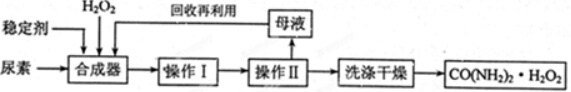
 H2O2+
H2O2+ 6H+=
6H+= Mn2++
Mn2++ O2↑+
O2↑+ 8H2O;
8H2O;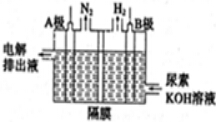
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
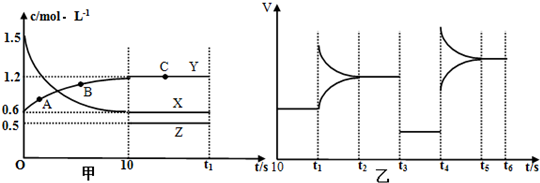
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com