
| A. | 地沟油的主要成分是高级脂肪酸甘油酯,可食用 | |
| B. | 高空臭氧层吸收太阳紫外线,保护地球生物;低空过量臭氧是污染气体,对人体有害 | |
| C. | NOx、SO2、CO2、PM2.5颗粒都会导致酸雨 | |
| D. | 石油化工中的分馏、裂化、裂解都是通过化学反应来获得轻质油、气体烯烃 |
分析 A.地沟油含有有害物质,不能够用做食用油;
B.在低空的臭氧是污染气体,人体吸收后加速氧化,而在高空的臭氧则是保护地球表面上的生物不受许多宇宙射线直接辐射的保护层;
C.二氧化碳不会导致酸雨产生,它含量过高导致温室效应;
D.分馏为物理变化,只得到饱和烃类物质.
解答 解:A.地沟油不能食用,故A错误;
B.高空臭氧层吸收太阳紫外线,保护地球生物;低空过量臭氧是污染气体,对人体有害,故B正确;
C.二氧化碳不会导致酸雨产生,它含量过高导致温室效应,故C错误;
D.分馏为物理变化,只得到饱和烃类物质,而裂化、裂解都是通过化学反应来获得轻质油、气体烯烃,故D错误;
故选B.
点评 本题考查了物质的用途,熟悉地沟油的成分、二氧化硫以及二氧化碳的性质、臭氧的作用、石油的分馏与裂化等概念是解题关键,题目难度不大.


科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
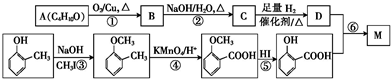
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 共价键 | H-H | N-H | N-N | N=N | N≡N |
| 键能/kJ•mol-1 | 436 | 391 | 159 | 418 | 945 |
| 次氯酸 | 磷酸 | 硫酸 | 高氧酸 | |
| 含氧酸 | Cl-OH |  |  |  |
| 非羟基氧原子数 | 0 | 1 | 2 | 3 |
| 酸性 | 弱酸 | 中强酸 | 强酸 | 最强酸 |
 .亚磷酸与过量的氢氧化钠溶液反应的化学方程式为H3PO3+2NaOH═Na2HPO3+2H2O.
.亚磷酸与过量的氢氧化钠溶液反应的化学方程式为H3PO3+2NaOH═Na2HPO3+2H2O. .铜晶体为面心立方最密集堆积,铜的原子半径为127.8pm,列式计算晶体铜的密度9.0 g/cm3.
.铜晶体为面心立方最密集堆积,铜的原子半径为127.8pm,列式计算晶体铜的密度9.0 g/cm3.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2种 | B. | 3种 | C. | 4种 | D. | 5种 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 金属离子 | Al(OH)3 | Fe(OH)2 | Fe(OH)3 | Mn(OH)2 |
| 沉淀完全的pH | 4.7 | 9.0 | 3.2 | 10.1 |
| 温度 溶解度 | 10 | 20 | 50 | 80 |
| Li2SO4 | 35.4 | 34.7 | 33.1 | 31.7 |
| Li2CO3 | 1.43 | 1.33 | 1.08 | 0.85 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 硝酸钾制备实验中,将NaNO3和KCl的混合液加热并浓缩至有晶体析出,趁热过滤时,可以分离出硝酸钾 | |
| B. | 重结晶过程中产生的母液虽然含有杂质,但仍应将母液收集起来,进行适当处理,以提高产率 | |
| C. | 甲装置可用于某些化学反应速率的测定.该装置气密性的检查如下:仪器组装好后,关闭分液漏斗活塞,将针筒活塞向外拉一段距离,然后松手,观察针筒是否能回到原来刻度处 | |
| D. | 乙装置可用来制取和检验二氧化硫气体漂白性,待滤纸颜色褪去后立即用浸有碱液的棉花堵住试管口 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 第三周期ⅣA族,p区 | B. | 第四周期ⅡA族,s区 | ||
| C. | 第四周期Ⅷ族,d区 | D. | 第四周期ⅡB族,s区 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com