
下列设备工作时,将化学能转化为电能的是()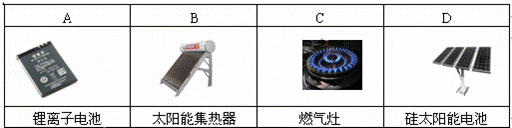
A. A B. B C. C D. D
科目:高中化学 来源: 题型:
下列各组离子在酸性溶液中可以大量共存的是( )
A. Ba2+ NO3﹣ NH4+ B. Na+ K+ SO32﹣
C. Ca2+ CO32﹣ Cl﹣ D. ClO﹣ Na+ NH4+
查看答案和解析>>
科目:高中化学 来源: 题型:
如图1所示,某同学设计了一个燃料电池并探究氯碱工业原理和粗铜的精炼原理,其中乙装置中X为阳离子交换膜.请按要求回答相关问题:
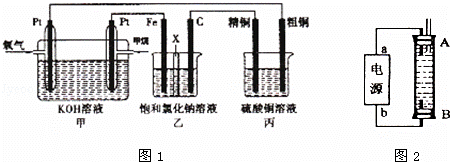
(1)甲烷燃料电池负极电极反应式是: ;
(2)石墨电极(C)的电极反应式为 ;
(3)若在标准状况下,有2.24L氧气参加反应,则乙装置中铁电极上生成的气体体积为 L;丙装置中阴极析出铜的质量为 g;
(4)某同学利甲烷燃料电池设计电解法制取漂白液或Fe(OH)2的实验装置(如图2所示).
若用于制漂白液时a为电池负极,电解质溶液最好用 .
若用于制Fe(OH)2,使用硫酸钠做电解质溶液,阳极选用铁作电极.
查看答案和解析>>
科目:高中化学 来源: 题型:
用FeCl3溶液腐蚀印刷电路板上的铜,所得的溶液中加入铁粉.对加入铁粉充分反应后的溶液分析合理的是()
A. 若无固体剩余,则溶液中一定有Fe3+
B. 若有固体存在,则溶液中一定有Fe2+
C. 若溶液中有Cu2+,则一定没有固体析出
D. 若溶液中有Fe2+,则一定有Cu析出
查看答案和解析>>
科目:高中化学 来源: 题型:
I.下列物质中属于强电解质的是 ;属于弱电解质的是 ;属于非电解质的是 .(填序号) ①氨气 ②氨水 ③盐酸 ④醋酸 ⑤硫酸钡 ⑥银 ⑦氯化钠 ⑧二氧化碳 ⑨醋酸铵 ⑩氢气
II.某反应体系中的物质有:Cr2(SO4)3、K2S2O8、K2Cr2O7、K2SO4、H2SO4、H2O.已知K2S2O8的氧化性比K2Cr2O7强.
(1)请将以上反应物与生成物编写成一个氧化还原反应方程式(不要求配平)
(2)反应中,被还原的物质是 是
(3)在酸性条件下K2Cr2O7与草酸(H2C2O4)反应的产物是:Cr2(SO4)3、CO2、K2SO4和H2O,则还原剂与氧化剂物质的量之比为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于化学基本原理和基本概念的几点认识中正确的是()
A. 胶体区别于其他分散系的本质特征是丁达尔现象
B. 强电解质溶液的导电能力强于弱电解质溶液
C. NaCl既可表示氯化钠的组成,又能表示其分子式
D. 一般认为沉淀离子浓度小于1.0×10﹣5mol/L时,则认为已经沉淀完全
查看答案和解析>>
科目:高中化学 来源: 题型:
Li~SO2电池具有输出功率高且低温性能好特点,其电解质为LiBr,溶剂是碳酸丙烯酯和乙腈,Li+可在其中移动.电池总反应式为:2Li+2SO2 Li2S2O4下列有关电池的说法正确的是()
Li2S2O4下列有关电池的说法正确的是()
A. 该电池总反应为可逆反应
B. 充电时阴极反应式为:Li++e﹣═Li
C. 放电时Li+向负极移动
D. 该电池电解质溶液可换成LiBr水溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
相等物质的量的CO和CO2相比较,下列有关叙述中正确的是()
①它们所含的分子数目之比为1:1
②它们所含的O原子数目之比为1:2
③它们所含的原子总数目之比为2:3
④它们所含的C原子数目之比为1:1
⑤它们的质量之比为7:11.
A. 仅①和④ B. 仅②和③ C. 仅④和⑤ D. ①②③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
利用下列装置进行相应实验,不能达到实验目的是()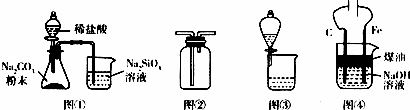
A. 图①装置可验证酸性:H2CO3>H2SiO3
B. 图②装置可用于收集气体H2、CO2、Cl2、NH3
C. 图③装置可用于分离互不相溶的两种液体
D. 图④装置可制备Fe(OH)2并能较长时间保持其颜色
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com