
下列有关说法正确的是
A.CaCO3(s)=CaO(s)+CO2(g)室温下不能自发进行,说明该反应的△H<0
B.镀锡铁制品镀层受损后,铁制品比受损前更容易生锈
C.N2(g)+3H2(g)?2NH3(g)△H<0,其他条件不变时升高温度,反应速率v(H2 )和H2的平衡转化率均增大
D.常温下,某溶液的PH=2,则该溶液一定是酸溶液
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:2016-2017学年河南省高二上期中化学卷(解析版) 题型:选择题
青铜器的制造是中华民族劳动人民智慧的结晶,成为一个时代的象征,但出土的青铜器大多受到环境腐蚀。如图为青铜器在潮湿环境中发生电化学腐蚀的原理示意图。环境中的Cl-扩散到孔口,并与各电极产物作用生成多孔粉状锈Cu2(OH)3Cl。下列说法不正确的
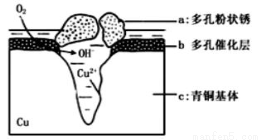
A.腐蚀过程中,负极c被氧化
B.环境中的Cl-扩散到孔口,并与正极反应产物和负极反应产物作用生成多孔粉状锈Cu2(OH)3Cl,其离子方程式为2Cu2++3OH-+Cl-=Cu2(OH)3Cl↓
C.若生成2.145gCu2(OH)3Cl,则理论上消耗标准状况氧气体积为0.448L
D.正极的电极反应式为:正极反应是O2+4e-+2H2O=4OH-
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高二上月考二化学卷(解析版) 题型:选择题
在NH4Cl与NH3·H2O组成的混合液中,下列关系一定正确的是
A.c(NH4+)>c(Cl—) B.c(H+)=c(OH—)
C.c(NH4+)+c(NH3·H2O)>c(Cl—) D.c(NH4+)>c(Cl—)+c(OH—)
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高二上月考二化学卷(解析版) 题型:选择题
一定量的锌粒与足量稀硫酸反应,向反应混合液中加入某些物质,下列判断正确的是
A.加入少量水,产生H速率减小,H2体积不变
B.加入NH4HSO4固体,产生H2速率不变,H2体积不变
C.加入CH3COONa固体,产生H2速率减小,H2体积减小
D.滴加少量CuSO4溶液,产生H2速率变大,H2体积减小
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高二上期中化学卷(解析版) 题型:填空题
研究硫元素及其化合物的性质具有重要意义。
Ⅰ.25℃,在0.10mol·L-1H2S溶液中,通入HCl气体或加入NaOH固体以调节溶液pH,溶液pH与c(S2-) 关系如图(忽略溶液体积的变化、H2S的挥发)。
①pH=13时,溶液中的c(H2S)+c(HS-)= mol·L-1.
②某溶液含0.020 mol·L-1Mn2+、0.10 mol·L-1H2S,当溶液pH= 时,Mn2+开始沉淀。[已知:Ksp(MnS)=2.8×10-13]
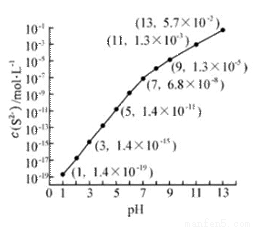
Ⅱ.在一定条件下,二氧化硫和氧气发生如下反应:2SO2(g)+O2(g) 2SO3(g)(Q>0)
2SO3(g)(Q>0)

(1)600℃时,在一密闭容器中,将二氧化硫和氧气混合,反应过程中SO2、O2、SO3物质的量变化如图,反应处于平衡状态的时间是____________。
(2)据图判断,反应进行至20min时,曲线发生变化的原因是______________(用文字表达)10min到15min的曲线变化的原因可能是______________(填写编号)。
a.加了催化剂 b.缩小容器体积 c.降低温度 d.增加SO3的物质的量.
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高二上期中化学卷(解析版) 题型:选择题
10mL浓度为1mol·L-1的盐酸与过量的锌粉反应,若加入适量的下列溶液,能减慢反应速率但又不影响氢气生成的是( )
A.KNO3 B.CH3COONa C.CuSO4 D.Na2CO3
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高二上期中化学卷(解析版) 题型:选择题
浓度均为0.10mol·L-1、体积均为V0的MOH和ROH分别加水稀释至体积V,pH随lg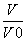 的变化如图所示,下列叙述错误的是
的变化如图所示,下列叙述错误的是
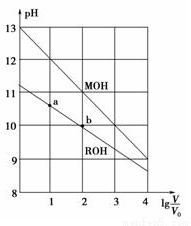
A.MOH的碱性强于ROH的碱性
B.ROH的电离程度:b点大于a点
C.若两溶液无限稀释,则它们的c(OH-)相等
D.当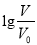 =2时,若两溶液同时升高温度,则
=2时,若两溶液同时升高温度,则 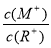 增大
增大
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高二上期中化学卷(解析版) 题型:填空题
T0C时,在一个体积为2L的容器中,A气体和B气体反应反应生成C气体,反应过程中A、B、C浓度变化如图所示.
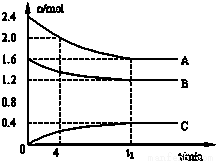
(1) 写出该反应的方程式:_______________
(2) 计算该温度下该反应的平衡常数:_______________
(3) 已知:K(300℃)>K(350℃),该反应是____________热反应.
(4) 0~4分钟时,B的平均反应速率为:_______________
(5) 到达平衡时A的转化率为:_______________
(6) 恒容条件下,下列措施中能使n(A)/n(C)降低的有____________.
A.充入氦气 B.使用催化剂
C.再充入2.4molA和1.6molB D.降低温度.
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江牡丹江高级中学高一上期中化学卷(解析版) 题型:选择题
已知反应:
①2FeCl3+2KI=2FeCl2+2KCl+I2
②2FeCl2+Cl2=2FeCl3
③I2+SO2+2H2O=H2SO4+2HI,判断下列物质的还原能力由强到弱的顺序是
A.I->Fe2+>Cl->SO2 B.Cl->Fe2+>SO2>I-
C.Fe2+>I->Cl->SO2 D.SO2>I->Fe2+>Cl-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com