
【题目】下列物质的分子中,键角最大的是( )
A. H2O B. BF3 C. CH4 D. NH3
科目:高中化学 来源: 题型:
【题目】下列有关电子云及示意图的说法正确的是( )
A. 电子云是笼罩在原子核外的云雾
B. 小黑点多的区域表示电子多
C. 小黑点疏的区域表示电子出现的机会少
D. 电子云是用高速照相机拍摄的照片
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以富含硫酸亚铁的工业废液为原料生产氧化铁的工艺如下(部分操作和条件略):
I.从废液中提纯并结晶出FeSO4·7H2O。
Ⅱ.将FeSO4·7H2O配制成溶液。
Ⅲ.FeSO4溶液与稍过量的NH4HCO3溶液混合,得到含FeCO3的浊液。
Ⅳ.将浊液过滤,用90℃热水洗涤沉淀,干燥后得到FeCO3固体。
V.煅烧FeCO3,得到Fe2O3固体。
已知:NH4HCO3在热水中分解。
(1)简述由硫酸亚铁晶体得到FeSO4·7H2O的主要操作步骤:___________________。
(2)Ⅱ中,需加一定量硫酸。同理,配制硫酸铝溶液时也需加入一定量的硫酸,请说出加入硫酸的作用,并写出相关的离子方程式:________________________。
(3)Ⅲ中,生成FeCO3的离子方程式是 ____________________。若FeCO3浊液长时间暴露在空气中,会有部分固体表面变为红褐色,该变化的化学方程式是____________________。
(4)IV中为什么用90℃热水洗涤沉淀?____________________。
(5)已知煅烧FeCO3的化学方程式是4 FeCO3+O2![]() 2Fe2O3+4CO2。现煅烧 464.0 kg的FeCO3,得到316.8 kg产品。若产品中杂质只有FeO,则用氧气将这些FeO氧化需要标况下氧气的体积是_________L。
2Fe2O3+4CO2。现煅烧 464.0 kg的FeCO3,得到316.8 kg产品。若产品中杂质只有FeO,则用氧气将这些FeO氧化需要标况下氧气的体积是_________L。
(摩尔质量/g·mol-1:FeCO3:116g·mol-1;Fe2O3:160g·mol-1;FeO:72g·mol-1)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】完全燃烧一定质量的无水乙醇,放出的热量为Q,为完全吸收生成的CO2,并使之生成正盐Na2CO3,消耗掉0.8mol/L NaOH溶液500mL,则燃烧1mol酒精放出的热量是( )
A. 0.2Q B. 0.1Q C. 5Q D. 10Q
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“84”消毒液和漂白粉都是氯气与碱反应在生活中的实际应用,下面说法错误的是( )
A.“84”消毒液有漂白和消毒作用
B.工业中将氯气通入石灰乳中制取漂白粉
C.漂白粉的有效成分是CaCl2和Ca(ClO)2
D.漂白粉在空气中久置失效
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向50mL NaOH溶液中逐渐通入一定量的CO2(假设溶液体积不变),随后取此溶液10mL,将其稀释至100mL,并向此稀释后的溶液中逐滴加入0.1mol·L﹣1的盐酸,产生CO2气体的体积(标准状况下)与所加入的盐酸的体积关系如图,下列分析错误的是( )
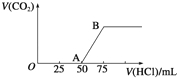
A.OA段所发生反应的离子方程式:H++OH﹣═H2O;CO32﹣+H+═HCO3-
B.NaOH在吸收CO2后,所得溶液的溶质为NaOH和Na2CO3,其物质的量浓度之比为1:1
C.产生的CO2体积(标准状况下)为0.056 L
D.原NaOH溶液的物质的量浓度为0.5 mol·L﹣1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com