
【题目】下列叙述正确的是
A.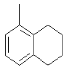 中所有的碳原子可能在同一平面上
中所有的碳原子可能在同一平面上
B.![]() 的一氯代物有4种
的一氯代物有4种
C.![]() 的命名为2,3-二甲基-1-丙醇
的命名为2,3-二甲基-1-丙醇
D.1mol![]() 与足量的NaOH溶液、溴水反应时,消耗NaOH和Br2的物质的量为4mol和2mol
与足量的NaOH溶液、溴水反应时,消耗NaOH和Br2的物质的量为4mol和2mol
【答案】D
【解析】
A.含有饱和碳原子,具有甲烷的结构特点,呈现四面体结构,因而该结构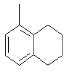 中所有碳原子不可能在同一平面上,故A错误;
中所有碳原子不可能在同一平面上,故A错误;
B.根据对称性可知,![]() 分子中含有3种氢原子,一氯代物有3种,故B错误;
分子中含有3种氢原子,一氯代物有3种,故B错误;
C.醇类命名选取含有羟基的最长碳链为主链,即为丁醇,在2号碳上含有羟基,在3号碳上含有甲基,正确命名为:3甲基2丁醇,故C错误;
D.该分子结构中含有2个酚羟基、1个羟基和1个酯基,能够与NaOH反应的有2个酚羟基和1个酯基,其中酯基水解后生成1个酚羟基和1个羧基,所以1mol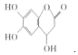 能够消耗4mol氢氧化钠,酚羟基邻位H原子可被溴水中的溴取代,该结构中有两个邻位H,则1mol有机物可与2mol溴反应,故D正确;
能够消耗4mol氢氧化钠,酚羟基邻位H原子可被溴水中的溴取代,该结构中有两个邻位H,则1mol有机物可与2mol溴反应,故D正确;
答案为D。


 学期复习一本通学习总动员期末加暑假延边人民出版社系列答案
学期复习一本通学习总动员期末加暑假延边人民出版社系列答案 芒果教辅暑假天地重庆出版社系列答案
芒果教辅暑假天地重庆出版社系列答案科目:高中化学 来源: 题型:
【题目】下列有关化学用语表示正确的是
A.HCO3-水解方程式:HCO3-+H+![]() H2CO3
H2CO3
B.水的电离方程式:H2O+H2O![]() H3O++OH-
H3O++OH-
C.向氯化银悬浊液中滴入KI溶液:Ag++I-== AgI↓
D.甲烷的燃烧热为-890.3 kJmol-1,则甲烷燃烧的热化学方程式可表示为;CH4(g)+2O2=CO2(g)+2H2O(g)ΔH=-890.3 kJmol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将 N2、H2 的混合气体分别充入甲、乙、丙三个容器中,进行合成氨反应,经过相同的一段时间后,测得反应速率分别为:甲:v(H2)=1 mol·L-1·min-1;乙:v(N2)=2 mol·L-1·min-1;丙:v(NH3)=3 mol·L-1·min-1。则三个容器中合成氨的反应速率( )
A.v(甲)>v(乙)>v(丙)B.v(乙)>v(丙)>v(甲)
C.v (丙)>v(甲)>v(乙)D.v(乙)>v(甲)>v(丙)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列表示对应化学反应的离子方程式正确的是( )
A.向稀HNO3中滴加Na2SO3溶液:SO![]() +2H+=SO2↑+H2O
+2H+=SO2↑+H2O
B.向Na2SiO3溶液中通入过量CO2:SiO![]() +CO2+H2O=H2SiO3↓+CO
+CO2+H2O=H2SiO3↓+CO![]()
C.向Al2(SO4)3溶液中加入过量的NH3·H2O:Al3++4NH3·H2O=AlO![]() +4NH
+4NH![]()
D.向CuSO4溶液中加入Na:2Na+Cu2++2H2O=2Na++Cu(OH)2↓+H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上以碳酸锰矿(主要成分为MnCO3,另含FeO、Fe2O3、CaO等杂质)为主要原料生产锰酸锂(LiMn2O4)的工艺流程如下:
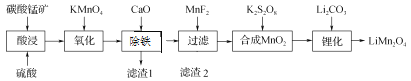
已知:部分离子沉淀的pH值。
离子 | 开始沉淀的pH值 | 沉淀完全时的pH值 |
Mn2+ | 8.8 | 10.8 |
Fe2+ | 7.5 | 9.5 |
Fe3+ | 2.2 | 3.5 |
(1) 为了提高碳酸锰矿浸岀的速率,在“酸浸”时可采取的措施有:①适当升高温度;②搅拌;③_____等。
(2) 氧化时发生的离子方程式:_________。
(3) 加入CaO“除铁”的原理是____________。
(4) 加入MnF2为了除去溶液中的Ca2+,若控制溶液中F-浓度为3×10-3 mol·L-1,则Ca2+的浓度为________mol·L-1[常温时,Ksp(CaF2)=2.7×10-11]。
(5) “锂化”是将MnO2和Li2CO3按4∶1的物质的量比配料,球磨3~5 h,然后升温至600~750 ℃,保温24 h,自然冷却至室温得产品。升温到515 ℃时,开始有CO2产生,比预计碳酸锂的分解温度(723 ℃)低得多。可能的原因是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(某化学兴趣小组制取氯酸钾和氯水并进行有关探究实验。
实验一 制取氯酸钾和氯水
利用下图所示的实验装置进行实验。

(1)制取实验结束后,取出B中试管冷却结晶,过滤,洗涤。该实验操作过程需要的玻璃仪器有________。
(2)若对调B和C装置的位置,________(填“能”或“不能”)提高B中氯酸钾的产率。
实验二 氯酸钾与碘化钾反应的研究
(3)在不同条件下KClO3可将KI氧化为I2或KIO3。该小组设计了系列实验研究反应条件对反应产物的影响,其中系列a实验的记录表如下(实验在室温下进行):
试管编号 | 1 | 2 | 3 | 4 |
0.20 mol·L-1 KI/mL | 1.0 | 1.0 | 1.0 | 1.0 |
KClO3(s)/g | 0.10 | 0.10 | 0.10 | 0.10 |
6.0 mol·L-1H2SO4/mL | 0 | 3.0 | 6.0 | 9.0 |
蒸馏水/mL | 9.0 | 6.0 | 3.0 | 0 |
实验现象 |
①系列a实验的实验目的是________________。
②设计1号试管实验的作用是________________。
③若2号试管实验现象为“黄色溶液”,取少量该溶液加入淀粉溶液显蓝色;假设氧化产物唯一,还原产物为KCl,则此反应的离子方程式为___________________________。
实验三 测定饱和氯水中氯元素的总量
(4)该小组设计的实验方案为使用下图装置,加热15.0 mL饱和氯水试样,测定产生气体的体积。此方案不可行的主要原因是__________________________。(不考虑实验装置及操作失误导致不可行的原因)

(5)根据下列资料,为该小组设计一个可行的实验方案(不必描述操作过程的细节):______________________________________________________________________。
资料:ⅰ.次氯酸会破坏酸碱指示剂;
ⅱ.次氯酸或氯气可被SO2、H2O2和FeCl2等物质还原成Cl-。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究电解质在水溶液中的平衡能了解它的存在形式,有重要的实际意义。

(1)常温下,向100mL0.01mol·L-1HA的溶液中逐滴加入0.02mol·L-1MOH溶液,所得溶液的pH随MOH溶液的体积变化如图所示(溶液体积变化忽略不计)。
①常温下,0.01mol·L-1HA溶液中由水电离出的c(H+)=_____mol·L-1。
②常温下一定浓度的MA稀溶液的pH=a,则a____7(填“>”、“<”或“=”),用离子方程式表示其原因为_____。
③X点时,溶液中c(H+)、c(M+)、c(A-)由大到小的顺序是_____。
④K点时,溶液中c(H+)+ c(M+)- c(OH-)=____molL-1。
(2)25 ℃时,已知Ka(CH3COOH)=1.75×10-5,Kb(NH3·H2O)=1.76×10-5。取浓度均为0.100 0 mol·L-1的醋酸溶液和氨水溶液各20.00 mL于锥形瓶中,分别用0.1000 mol·L-1NaOH溶液、0.1000 mol·L-1盐酸进行滴定,滴定过程中pH随滴加溶液体积变化关系如图所示。
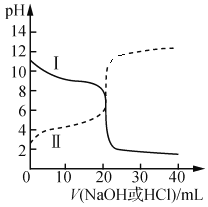
①从曲线I可知,该滴定操作时,应选______作为指示剂。
②在曲线Ⅱ,当滴加溶液到10.00 mL时:
c(CH3COO-)+c(OH-) ___ c(H+)+c(CH3COOH) (填“>”、“<”或“=”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】葛根大豆苷元![]() 用于治疗高血压引起的头疼、突发性耳聋等症,其合成路线如下:
用于治疗高血压引起的头疼、突发性耳聋等症,其合成路线如下:
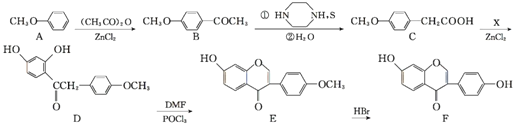
![]() 化合物B中的含氧官能团有 ______
化合物B中的含氧官能团有 ______ ![]() 填官能团名称
填官能团名称![]() ;
;
![]() 已知X为
已知X为![]() ,写出该反应的化学方程式 ______ ;
,写出该反应的化学方程式 ______ ;
![]() 已知D与
已知D与![]() 二甲基甲酰胺,结构简式为
二甲基甲酰胺,结构简式为![]()
![]() 在
在![]() 三氯氧磷
三氯氧磷![]() 的催化下反应生成E,同时还生成
的催化下反应生成E,同时还生成![]() 和另一种有机物,写出该有机物的分子式 ______ ;
和另一种有机物,写出该有机物的分子式 ______ ;
![]() 的分子式为 ______ ,由E生成F的反应类型为 ______ ;
的分子式为 ______ ,由E生成F的反应类型为 ______ ;
![]() 的芳香同分异构体中苯环上有三个取代基,并且既能发生银镜反应,又能发生水解反应的有 ______ 种,其中核磁共振氢谱为4组峰,且峰面积比为6:2:1:1的为 ______
的芳香同分异构体中苯环上有三个取代基,并且既能发生银镜反应,又能发生水解反应的有 ______ 种,其中核磁共振氢谱为4组峰,且峰面积比为6:2:1:1的为 ______ ![]() 写出其中一种的结构简式
写出其中一种的结构简式![]()
![]() 根据已有知识并结合相关信息,写出以
根据已有知识并结合相关信息,写出以![]() 和
和![]() 为原料制备
为原料制备![]() 的合成路线流程图
的合成路线流程图![]() 无机试剂任用
无机试剂任用![]() 合成路线流程图示例如下: ____________
合成路线流程图示例如下: ____________
![]() 。
。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关系式错误的是![]()
A.![]() 的水溶液:
的水溶液:![]()
B.等浓度的HCN溶液与NaOH溶液等体积混合,所得溶液![]() ,则溶液中离子浓度:
,则溶液中离子浓度:![]()
C.![]() 某一元酸HA溶液和
某一元酸HA溶液和![]() 溶液等体积混合的溶液中:
溶液等体积混合的溶液中:![]()
D.两种弱酸HX和HY混合后,溶液中的![]() 为
为![]() 为电离平衡常数
为电离平衡常数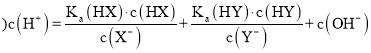
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com