
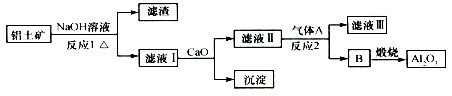
| A. | 气体A一定为HCl | B. | 滤液Ⅰ中溶质可能含NaAlO2 | ||
| C. | 沉淀的主要成分不是硅酸钙 | D. | 反应1、反应2均是氧化还原反应 |
分析 SiO2和盐酸不反应,Fe2O3和氢氧化钠不反应而氧化铝能反应,向偏铝酸钠中通入过量的二氧化碳可以生成氢氧化铝沉淀.
铝土矿中加入氢氧化钠溶液,氧化铝和二氧化硅与氢氧化钠反应生成偏铝酸钠和硅酸钠,则滤液Ⅰ为NaAlO2和硅酸钠,加入氢氧化钙,生成硅酸钙沉淀,滤液Ⅱ为偏铝酸钠,可通入二氧化碳气体,生成B为氢氧化铝,煅烧可生成氧化铝,以此解答该题.
解答 解:铝土矿中加入氢氧化钠溶液,氧化铝和二氧化硅与氢氧化钠反应生成偏铝酸钠和硅酸钠,则滤液Ⅰ为NaAlO2和硅酸钠,加入氢氧化钙,生成硅酸钙沉淀,滤液Ⅱ为偏铝酸钠,可通入二氧化碳气体,生成B为氢氧化铝,煅烧可生成氧化铝,
A.气体A应为二氧化碳,故A错误;
B.滤液Ⅰ为NaAlO2和硅酸钠,故B正确;
C.由以上分析可知沉淀为硅酸钙,故C错误;
D.反应2为复分解反应,化合价没有发生变化,不是氧化还原反应,故D错误.
故选B.
点评 本题考查二氧化硅和铝及其化合物的性质,为高频考点,侧重与学生的分析能力和实验能力的考查,把握流程中发生的化学反应为解答的关键,难度不大.


 名校通行证有效作业系列答案
名校通行证有效作业系列答案科目:高中化学 来源: 题型:解答题
 (1)同一物质存在气态的熵值最大,液态的熵值次之,固态的熵值最小.若同温同压下,一个反应生成物气体的体积等于反应物气体的体积就可粗略认为该反应的熵变为0.某化学兴趣小组,专门研究了氧族元素及其某些化学物的部分性质.所查资料如下:
(1)同一物质存在气态的熵值最大,液态的熵值次之,固态的熵值最小.若同温同压下,一个反应生成物气体的体积等于反应物气体的体积就可粗略认为该反应的熵变为0.某化学兴趣小组,专门研究了氧族元素及其某些化学物的部分性质.所查资料如下:查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 反应2Mg(s)+CO2(g)=C(s)+2MgO(s)能自发进行,则该反应的△H<0 | |
| B. | 为处理银器表面的黑斑(Ag2S),将银器浸于铝质容器里的食盐水中并与铝接触 | |
| C. | 常温下,将稀CH3COONa溶液加水稀释后,溶液中n(H+)•n(OH-)不变 | |
| D. | 在盛有Ca(OH)2悬浊液的绝热密闭容器中,加入少量的CaO粉末后,溶液中Ca2+数目不变,pH降低 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分液、蒸馏、分液 | B. | 分液、蒸馏、萃取 | C. | 蒸馏、蒸馏、萃取 | D. | 蒸馏、分液、萃取 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | +5 | B. | +4 | C. | +3 | D. | +2 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe(OH)3胶体带正电荷,因此能发生电泳现象 | |
| B. | Fe(OH)3胶体与FeCl3溶液的本质区别是胶体粒子直径在1-100nm之间 | |
| C. | 将FeCl3溶液加入到沸水中能制得Fe(OH)3胶体 | |
| D. | Fe(OH)3胶体和CuSO4溶液都能发生丁达尔现象 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com