
设NA代表阿伏加德罗常数的数值,下列说法正确的是
A.标准状况下,1molCO2、CO的混合气中含有的氧原子数为1.5NA
B.标准状况下,11.2LCCl4所含的分子数为0.5NA
C.25℃,1.01×105Pa,66gCO2中所含原子数为4.5NA
D.1mol•L﹣1CuCl2溶液中含有的氯离子数为2NA
 高效智能课时作业系列答案
高效智能课时作业系列答案 捷径训练检测卷系列答案
捷径训练检测卷系列答案 小夫子全能检测系列答案
小夫子全能检测系列答案科目:高中化学 来源:2016-2017学年遵义市高二上学期期中考试(理科)化学试卷 题型:选择题
已知:C(s)+CO2(g) 2CO(g)△H>0。该反应的达到平衡后,下列条件
2CO(g)△H>0。该反应的达到平衡后,下列条件
有利于反应向正方向进行的是
A.升高温度和 减小压强
减小压强
B.降低温度和减小压强
C.降低温度和增大压强
D.升高温度和增大压强
查看答案和解析>>
科目:高中化学 来源:2017届安徽省高三上第二次月考化学试卷(解析版) 题型:实验题
某化学小组探究酸性条件下NO3-、SO42-、Fe3+三种微粒的氧化性强弱,设计如下实验(夹持仪器已略去,装置的气密性已检验)。(忽略氧气对反应的影响)
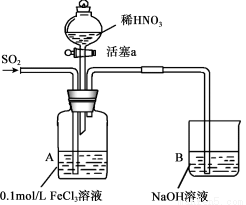
实验记录如下:
实验序号 | 实验操作 | 实验现象 |
I | 向A装置中通入一段时间的SO2气体。 | A中黄色溶液迅速变成深红棕色,最终变为浅绿色。 |
II | 取出少量A装置中的溶液,先加入KSCN溶液,再加入BaCl2溶液。 | 加入KSCN溶液后溶液不变色,再加入BaCl2溶液产生白色沉淀。 |
III | 打开活塞a,将过量稀HNO3加入装置A中,关闭活塞a | A中浅绿色溶液最终变为黄色。 |
IV | 取出少量A装置中的溶液,加入KSCN溶液;向A装置中通入空气。 | 溶液变为红色;液面上方有少量红棕色气体生成。 |
请回答下列问题:
(1)配制FeCl3溶液时,常常加入盐酸,目的是(用化学方程式和简单文字叙述): 。
(2)资料表明,Fe3+能与SO2结合形成深红棕色物质Fe(SO2)63+,反应方程式为: Fe3+ + 6SO2  Fe(SO2)63+。请用化学平衡移动原理解释实验I中溶液颜色变化的原因 。
Fe(SO2)63+。请用化学平衡移动原理解释实验I中溶液颜色变化的原因 。
(3)实验II中发生反应的离子方程式是 。
(4)实验III中,浅绿色溶液变为黄色的原因是(用离子方程式表示) 。
(5)实验IV中液面上方有少量红棕色气体生成,发生反应的方程式是 。
(6)综合上述实验得出的结论是:在酸性条件下,NO3-、SO42-、Fe3+三种微粒的氧化性由强到弱的顺序是: 。
查看答案和解析>>
科目:高中化学 来源:2017届安徽省高三上第二次月考化学试卷(解析版) 题型:选择题
下列有关化学用语表示正确的是( )
A.二氧化硅的分子式 SiO2
B.质子数为53,中子数为78的碘原子 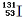
C.羟基的电子式 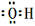
D.次氯酸的结构式:H﹣Cl﹣O
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省成都市高一上学期10月月考化学试卷 题型:选择题
在标准状况下,将aLHCl(气)溶于1L水中(水的密度为1g•c m﹣3),得到的盐酸的密度为bg•mL﹣1,质量分数为w,物质的量浓度为cmol•
m﹣3),得到的盐酸的密度为bg•mL﹣1,质量分数为w,物质的量浓度为cmol• L﹣1则下列关系式中不正确的是
L﹣1则下列关系式中不正确的是
A.w=
B.w=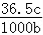
C.C=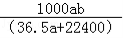
D.b=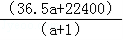
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省成都市高一上学期10月月考化学试卷 题型:选择题
下图是某同学用500mL容量瓶配制0.10mol·L-1Na2CO3溶液的步骤:

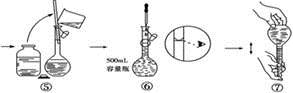
该同学的错误是
A. ①⑤⑥
B. ②④⑦
C. ①⑥
D. ⑤⑥⑦
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省成都市高二10月阶段性考试化学试卷 题型:填空题
合成氨是人类科学技术上的一项重大突破,其反应原理为N2(g)+3H2(g) 2NH3(g)ΔH=-92.4kJ·mol-1。一种工业合成氨的简式流程图如下:
2NH3(g)ΔH=-92.4kJ·mol-1。一种工业合成氨的简式流程图如下:
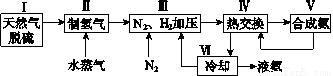
(1)天然气中的H2S杂质常用氨水吸收,产物为NH4HS。一定条件下向NH4HS溶液中通入空气,得到单质硫并使吸收液再生,写出再生反应的化学方程式:_______________________。
(2)步骤Ⅱ中制氢气的原理如下:
①CH4(g)+H2O(g) CO(g)+3H2(g)△H=+206.4kJ·mol-1
CO(g)+3H2(g)△H=+206.4kJ·mol-1
②CO(g)+H2O(g) CO2(g)+H2(g)△H=-41.2kJ·mol-1
CO2(g)+H2(g)△H=-41.2kJ·mol-1
对于反应①,一定可以提高平衡体系中H2的百分含量,又能加快反应速率的措施是____________。
a.升高温度b.增大水蒸气浓度c.加入催化剂d.降低压强
利用反应②,将CO进一步转化,可提高H2的产量。若1molCO和H2的混合气体(CO的体积分数为20%)与H2O反应,得到1.18molCO、CO2和H2的混合气体,则CO的转化率为__________。
(3)图(a)表示500℃、60.0MPa条件下,原料气投料比与平衡时NH3体积分数的关系。根据图中a点数据计算N2的平衡体积分数:____________。
(4)依据温度对合成氨反应的影响,在图(b)坐标系中,画出一定条件下的密闭容器内,从通入原料气开始,随温度不断升高,NH3物质的量变化的曲线示意图。


(a)(b)
(5)上述流程图中,使合成氨放出的能量得到充分利用的主要步骤是(填序号)________。简述本流程中提高合成氨原料总转化率的方法:______________________________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省成都市高二10月阶段性考试化学试卷 题型:选择题
NA为阿伏加德罗常数,下列叙述错误的是
A. 28gC2H4和C4H8混合气体中含有氢原子总数为4NA
B. 常温常压下,Cu-Zn原电池中,正极产生1.12LH2时,转移的电子数应小于0.1NA
C. 15g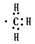 含有的电子数为9NA
含有的电子数为9NA
D. 2.1gDTO中所含中子数为NA
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高二上学期第二次月考化学试卷 题型:选择题
下列叙述正确的是
A.氢氧化铝.碳酸钠都是常见的胃酸中和剂
B.长期摄入肉.蛋.鱼偏多易导致血液偏酸性
C.碘酒中的碘因有还原性而起到杀菌消毒作用
D.碘盐.铁强化酱油等营养强化剂适合所有人食用
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com