
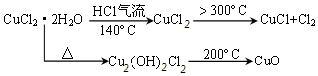
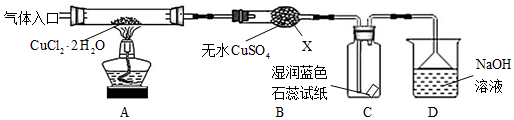
���� �ȷֽ�CuCl2•2H2O�Ʊ�CuCl��Ϊ����ˮ�⣬�������ͨ��HCl���壬Ȼ�����A���Թܣ�XΪ���θ���ܣ�X����ˮ����ͭ��������֪CuCl2•2H2O�ֽ�����ˮ���� ����300�棬����2CuCl2$\frac{\underline{\;����300��\;}}{\;}$2CuCl+Cl2������ �����л���Cl2������C��ʯ����ֽ����Ϊ��ɫ������ɫ��D��NaOH��Һ����β����ȡ��CuCl��Ʒ����ʵ�飬�������к���������CuCl2��CuO���ʣ�����CuCl2���¶Ȳ��������ʱ�䲻���йأ�����CuO��û����HCl�ķ�Χ�м��Ȼ���δ���Թ���ȴ��ֹͣͨ��HCl�����йأ��Դ������
��� �⣺��1�������������֪������X������Ϊ���θ���ܣ�
�ʴ�Ϊ�����θ���ܣ�
��2��ʵ�������������ɣ��ȼ���װ�õ������ԣ����ȷֽ�CuCl2•2H2O�Ʊ�CuCl����ֹCuCl��������Cu+ˮ�����Ա���Ҫ�ȸ���װ���е�������ˮ������ż��ȣ���Ҫ��HCl�����м����Ʊ�����Ӧ��������Ϩ��ƾ��ƣ�Ӧ��Ҫ����ͨ�뵪��ֱ��װ�����У����Բ���˳��Ϊ����-��-��-��-�ݣ�
�ʴ�Ϊ����-��-�ڣ�
��3��B���а�ɫ��Ϊ��ɫ��˵����ˮ���ɣ������л���Cl2������C��ʯ����ֽ����Ϊ��ɫ������ɫ��
�ʴ�Ϊ���ȱ��ɫ����ɫ��
��4��D����Cl2��NaOH��Ӧ�����Ȼ��ơ��������ƺ�ˮ����Ӧ�����ӷ���ʽΪCl2+2OH-=Cl-+ClO-+H2O��
�ʴ�Ϊ��Cl2+2OH-=Cl-+ClO-+H2O��
��5������2CuCl2$\frac{\underline{\;����300��\;}}{\;}$2CuCl+Cl2����������CuCl2˵��CuCl2û�з�Ӧ��ȫ���ֽ��¶Ȳ��ߣ�
�ʴ�Ϊ������ʱ�䲻����¶�ƫ�ͣ�
������������ͭ��˵��CuCl�����������Ų�����CuO��˵��װ������������������û����HCl�ķ�Χ�м��Ȼ���δ���Թ���ȴ��ֹͣͨ��HCl���壻
�ʴ�Ϊ��HCl�������㣻
��6����Cu2��OH��2Cl 2����CuO�Ļ�ѧ����ʽΪ��Cu2��OH��2Cl2�T2CuO+2HCl����
�ʴ�Ϊ��Cu2��OH��2Cl2�T2CuO+2HCl����
���� ���⿼�����ʵ��Ʊ�ʵ�飬Ϊ��Ƶ���㣬�����Ʊ�ʵ��ԭ����ʵ��װ�õ����á�Ԫ�ػ�����֪ʶΪ���Ĺؼ������ط�����ʵ�������Ŀ��飬ע��Ԫ�ػ�������ʵ�����ϵ�ѵ������5��Ϊ�����ѵ㣬��Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ƫ�� | B�� | ƫС | C�� | ��Ӱ�� | D�� | ��ȷ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| Ԫ�ش��� | X | Y | Z | W | Q |
| ԭ�Ӱ뾶��nm�� | 0.073 | 0.077 | 0.099 | 0.102 | 0.118 |
| ��Ҫ���ϼ� | -2 | +4��-4 | -1 | +6��-2 | +3 |
| A�� | ���ʷе㣺W��Q��Z | |
| B�� | W��Q�γɵij�������������ȶ�������ˮ��Һ�� | |
| C�� | Z�ĺ���������Դ���W�ĺ���������� | |
| D�� | X��Y��W����Ԫ������֮������Թ��ۼ��γ�AB2�͵Ļ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
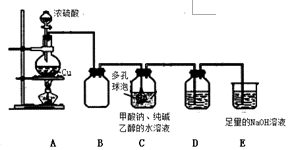 ��֪���١������������ƣ�Na2S2O4����һ�ְ�ɫ��ĩ��������ˮ���������Ҵ�����4HCl+2Na2S2O4�T4NaCl+S��+3SO2��+2H2OijС���������ʵ�飺
��֪���١������������ƣ�Na2S2O4����һ�ְ�ɫ��ĩ��������ˮ���������Ҵ�����4HCl+2Na2S2O4�T4NaCl+S��+3SO2��+2H2OijС���������ʵ�飺| ���� | ���� | ���� | ԭ�� |
| Na2S2O4 Ϊǿ �������Σ����� ҺΪ���ԣ� | ȡ������Һ���Թ��У� �μ���ɫˮ����Һ | ��Һ�� ����ɫ | S2O42-ˮ�⣬ʹ��Һ�ɼ��� |
| Na2S2O4 �� SΪ+3 �ۣ����н�ǿ �Ļ�ԭ�ԣ� | ȡ������Һ���Թ��У� �μӹ���������ˮ���� �μ� BaCl2 �� | �а�ɫ������ �� | �÷�Ӧ�����ӷ���ʽΪ��4H2O+S2O42-+3Cl2=2SO42-+6Cl-+8H+ ��Ba2++SO42-=BaSO4���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 2.24LH2O���еķ���������0.1NA | |
| B�� | 1.12LO2��1.12LN2����ԭ����һ����� | |
| C�� | ������ΪNA��CO��������Ϊ28�� | |
| D�� | 500mL2mol/L���Ȼ�����Һ��Cl��ĿΪNA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Na��NaOH��Na2CO3��NaCl | B�� | Al��Al2O3��Al��OH��3��AlCl3 | ||
| C�� | Cu��CuCl2��Cu��OH��2��CuSO4 | D�� | Fe��FeCl2��Fe��OH��2��Fe��OH��3 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com