
| A. | CH3COOH电离程度变大 | B. | 溶液pH变大 | ||
| C. | 溶液中c(H+)减小 | D. | 溶液的导电能力减弱 |
分析 CH3COOH溶液加水稀释,平衡向正反应方向移动,电离程度减小,溶液的pH增大,导电能力减弱,溶液中c(H+)减小;CH3COOH溶液加入少量CH3COONa晶体时平衡向逆反应方向移动,电离程度减小,溶液的PH增大,导电能力增强,溶液中c(H+)减小.
解答 解:A.CH3COOH溶液加水稀释,平衡向正反应方向移动,电离程度增大,加入少量CH3COONa晶体时平衡向逆反应方向移动,电离程度减小,故A错误;
B.CH3COOH溶液加水稀释,平衡向正反应方向移动,溶液的PH增加,CH3COOH溶液加入少量CH3COONa晶体时平衡向逆反应方向移动,溶液的pH增加,故B正确;
C.加水稀释,促进醋酸电离,但溶液中氢离子浓度减小,加入少量CH3COONa晶体时平衡向逆反应方向移动,电离程度减小,氢离子浓度减小,温度不变,水的离子积常数不变,所以氢氧根离子浓度增大,故C正确;
D.CH3COOH溶液加水稀释,离子浓度减小,溶液的导电能力减弱,加入少量CH3COONa晶体时,离子浓度增大,溶液的导电能力增强,故D错误;
故选BC.
点评 本题考查外界条件对电离平衡的影响,重点考查离子浓度以及同离子效应对电离平衡的影响,注意总结影响因素以及平衡移动的方向的判断.


 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 沸点:CO>N2 | B. | 水溶性:HCl>H2S>SO2 | ||
| C. | 还原性:HF>HCl>HBr>HI | D. | 沸点:HF>H2O>NH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 同周期元素的电子层数都相同 | |
| B. | 同族元素的最外层电子数一定相同 | |
| C. | 最外层电子数相同的元素都在同一族 | |
| D. | 周期表是按相对原子质量逐渐增大的顺序从左到右排列的 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 mol NaHSO4晶体中离子总数为2NA | |
| B. | 4.4g 14CO2含中子数为2.4NA | |
| C. | 0.3mol•L-1的NH4NO3溶液中含有的NH4+数目为0.3NA | |
| D. | 1 molFe在氧气中燃烧失去的电子数为3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C$\stackrel{在空气中燃烧}{→}$ CO$\stackrel{CuO△}{→}$ CO2$\stackrel{NaOH溶液}{→}$ Na2CO3 | |
| B. | Cu$\stackrel{AgNO_{3}溶液}{→}$ Cu(NO3)2溶液$\stackrel{NaOH溶液}{→}$ Cu(OH)2 | |
| C. | Fe $\stackrel{点燃}{→}$ Fe2O3$\stackrel{H_{2}SO_{4}溶液}{→}$ Fe2(SO4)3溶液 | |
| D. | CaO$\stackrel{H_{2}O}{→}$ Ca(OH)2溶液$\stackrel{Na_{2}CO_{3}溶液}{→}$ NaOH溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 不能确定HCO3-离子是否存在 | B. | 可能有CO32-离子 | ||
| C. | 一定有Cl-离子存在 | D. | 一定有SO42-离子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| J | ||||
| R |
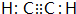 .
.| 选项 | a | b | c | d |
| x | 温度 | 温度 | 加入氧气 | 加入乙的物质 |
| y | 乙的物质的量 | 平衡常数K | 乙的转化率 | 生成物物质的量总和 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com