
工业从铝土矿(主要成分是Al2O3·xH2O、SiO2、Fe2O3等)提取纯Al2O3做冶炼铝的原料,提取时操作过程如下图,图中操作错误的是( )
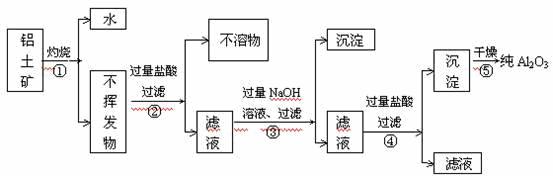
A ④⑤ B ③④ C ②⑤ D ①②
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
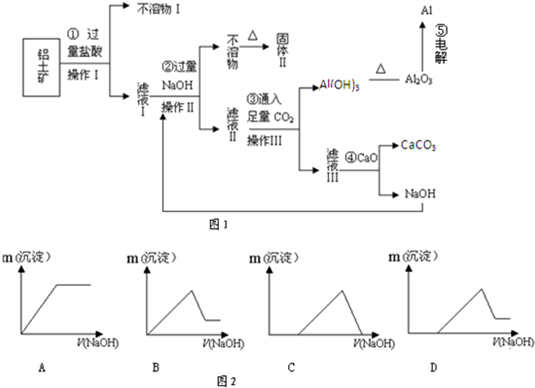
(26分) (1)铝土矿(主要成分为Al2O3,还含有SiO2、Fe2O3)是工业上制备氧化铝的主要原料。工业上提取氧化铝的工艺流程如下:
① 沉淀 A、B的成分分别是 、 ;步骤②中的试剂a是 ;
② 试写出步骤③中发生反应的离子方式 、 ;
③简述检验所得滤液甲中存在Fe3+的操作方法:__________ _。
(2)用含少量铁的氧化铜制取氯化铜晶体(CuCl2·xH2O)。有如下操作:
已知:在pH为4~5时,Fe3+几乎完全水解而沉淀,Cu2+却不水解。
① 加热酸溶过程中发生反应的化学方程式有: 。
② 氧化剂A可选用 (填编号,下同)。
A.KMnO4 B. HNO3 C. Cl2
③ 要得到较纯的产品,试剂B可选用 。
A. NaOH B. CuO C.FeO
④ 试剂B的作用是 。
A. 使Cu2+完全沉淀 B. 使Fe3+完全沉淀
C. 降低溶液的pH D. 提高溶液的pH
⑤ 从滤液经过结晶得到氯化铜晶体的方法是 (按实验先后顺序选填编号)。
A. 过滤 B. 蒸发至干 C. 冷却 D. 蒸发浓缩
查看答案和解析>>
科目:高中化学 来源:2012届高三上学期九月份月考化学试卷(必修1第1-3章部分内容) 题型:实验题
(26分) (1)铝土矿(主要成分为Al2O3,还含有SiO2、Fe2O3)是工业上制备氧化铝的主要原料。工业上提取氧化铝的工艺流程如下: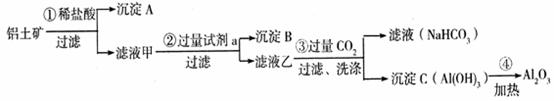
① 沉淀 A、B的成分分别是 、 ;步骤②中的试剂a是 ;
② 试写出步骤③中发生反应的离子方式 、 ;
③简述检验所得滤液甲中存在Fe3+的操作方法:__________ _。
(2)用含少量铁的氧化铜制取氯化铜晶体(CuCl2·xH2O)。有如下操作: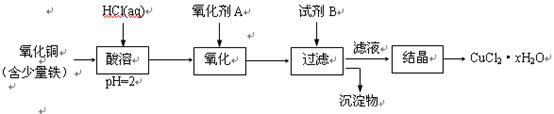
已知:在pH为4~5时,Fe3+几乎完全水解而沉淀,Cu2+却不水解。
① 加热酸溶过程中发生反应的化学方程式有: 。
② 氧化剂A可选用 (填编号,下同)。
A.KMnO4 B. HNO3 C. Cl2
③ 要得到较纯的产品,试剂B可选用 。
A. NaOH B. CuO C.FeO
④ 试剂B的作用是 。
A. 使Cu2+完全沉淀 B. 使Fe3+完全沉淀
C. 降低溶液的pH D. 提高溶液的pH
⑤ 从滤液经过结晶得到氯化铜晶体的方法是 (按实验先后顺序选填编号)。
A. 过滤 B. 蒸发至干 C. 冷却 D. 蒸发浓缩
查看答案和解析>>
科目:高中化学 来源:2011-2012学年高三上学期九月份月考化学试卷(必修1第1-3章部分内容) 题型:选择题
(26分) (1)铝土矿(主要成分为Al2O3,还含有SiO2、Fe2O3)是工业上制备氧化铝的主要原料。工业上提取氧化铝的工艺流程如下:
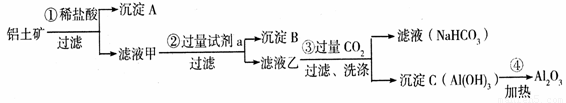
① 沉淀 A、B的成分分别是 、 ;步骤②中的试剂a是 ;
② 试写出步骤③中发生反应的离子方式 、 ;
③简述检验所得滤液甲中存在Fe3+的操作方法:__________ _。
(2)用含少量铁的氧化铜制取氯化铜晶体(CuCl2·xH2O)。有如下操作:
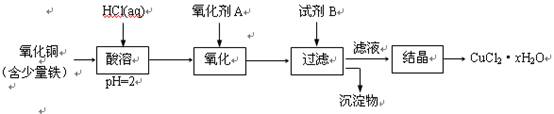
已知:在pH为4~5时,Fe3+几乎完全水解而沉淀,Cu2+却不水解。
① 加热酸溶过程中发生反应的化学方程式有: 。
② 氧化剂A可选用 (填编号,下同)。
A.KMnO4 B. HNO3 C. Cl2
③ 要得到较纯的产品,试剂B可选用 。
A. NaOH B. CuO C.FeO
④ 试剂B的作用是 。
A. 使Cu2+完全沉淀 B. 使Fe3+完全沉淀
C. 降低溶液的pH D. 提高溶液的pH
⑤ 从滤液经过结晶得到氯化铜晶体的方法是 (按实验先后顺序选填编号)。
A. 过滤 B. 蒸发至干 C. 冷却 D. 蒸发浓缩
查看答案和解析>>
科目:高中化学 来源: 题型:
工业上从铝土矿(主要成分是Al2O3,含SiO2、Fe2O3、MgO等杂质)中提取氧化铝的两种流程如下:

请回答下列问题:
(1)流程甲加入盐酸后生成Al3+的离子方程式为 。
(2)滤液E、K中溶质的主要成份是________(填化学式)。
(3)流程甲加入盐酸得到滤液B中含有 Fe3+、 Cl—等多种微粒,据此回答下列问题。
①验证其中含Fe3+,可取少量滤液并加入________(填试剂名称)。
 ②用FeCl3溶液腐蚀印刷电路铜板的化学方程式为:
②用FeCl3溶液腐蚀印刷电路铜板的化学方程式为:
。
若将该反应设计成原电池,如右图所示,则正极的电极
反应式为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com