
�о�NO2����CO�ȴ�����Ⱦ����Ĵ���������Ҫ���塣
���÷�Ӧ6NO2(g)��8NH3(g) 7N2(g)��12 H2O(g)�ɴ���NO2��700��ʱ�����ݻ�Ϊ2L���ܱ������г���һ������NO2��NH3, ��Ӧ�����вⶨ�IJ������ݼ��±�
7N2(g)��12 H2O(g)�ɴ���NO2��700��ʱ�����ݻ�Ϊ2L���ܱ������г���һ������NO2��NH3, ��Ӧ�����вⶨ�IJ������ݼ��±�
| ��Ӧʱ��/min | n(NO2)/mol | n(NH3)/ mol |
| 0 | 1.20 | 1.60 |
| 2 | 0.90 | |
| 4 | | 0.40 |
 CH3OH��g����200��ʱ������һ�����������ܱ�����������г���һ������CO��H2����������Ӧ,ѹ���������ݻ�Ϊԭ����һ�룬ƽ�⽫ �ƶ������������ң�������CO��Ũ�Ƚ� ������С�����䣩
CH3OH��g����200��ʱ������һ�����������ܱ�����������г���һ������CO��H2����������Ӧ,ѹ���������ݻ�Ϊԭ����һ�룬ƽ�⽫ �ƶ������������ң�������CO��Ũ�Ƚ� ������С�����䣩 ��1�� 0.1mol/(L��min) K={C7(N2)��C12(H2O)}/{C6(NO2)��C8(NH3)} 75�G
��2��a b ��3������ ����
���������������1���ɿ�ʼ��2����ʱ��n(NO2)=0.3mol,��n(NH3)=(8/6)��0.4mol.V(NH3)= {��n(NH3)/V}/��t=(0.4mol/2L)��2min=0.1mol/(L��min).��ѧƽ�ⳣ���ǿ��ܷ�Ӧ�ﵽ��ѧƽ��ʱ��������Ũ����ָ���ij˻������Ӧ��Ũ����ָ���˻��ıȡ���K={C7(N2)��C12(H2O)}/{C6(NO2)��C8(NH3)}����Ӧ���е� 4minʱ���÷�Ӧ�ﵽƽ��״̬����ʱ��n(NH3)=1.60-0.4=1.20��mol������n(NO2)=6/8��n(NH3)="(" 6/8)��1.20mol=0.9mol.����NO2��ת����Ϊ��(0.9mol/1.2mol)��100�G=75�G.
��2��a���ڸ÷�Ӧ�Ǹ���Ӧǰ������������ȵĿ��淴Ӧ�����Ե���Ӧ�ﵽ��ѧƽ��ʱ��ϵ��ѹǿ���䡣��ȷ��bƽ��ʱ��Ӧ������Ũ�ȱ��ֲ��䡣��ΪNO2�Ǻ���ɫ���壬���Դﵽƽ��ʱ���������ɫ���ֲ��䡣��ȷ��c���ڷ�Ӧ���������غ㶨�ɡ���ϵ���ݻ����䡣���������Ƿ�Ӧ��Ҳ�����Ƿ�Ӧ�Ƿ�ﵽƽ�⡣��ϵ���ܶȶ����ᷢ���ı䡣����D�κ�ʱ��ÿ����1 mol NO2��ͬʱ����2 mol H2O�����Ƿ�Ӧ������Ӧ������С��뷴Ӧ�Ƿ�ﵽƽ���ء���������ѡ��Ϊ��a b.��3������Ӧ�ﵽ��ѧƽ��ʱѹ�������������ѹǿ����ѧƽ�������������С�ķ����ƶ���Ҳ����������Ӧ�����ƶ�����ʱ��Ӧ������Ũ�ȶ�����
���㣺���黯ѧ��Ӧ���ʵļ��㡢��ѧƽ�ⳣ������������Ի�ѧƽ���Ӱ��ȵ�֪ʶ��


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
һ���¶��£���2L�ܱ�������NO2��O2�ɷ������з�Ӧ�� 4NO2(g)+O2(g) 2N2O5(g)+5286 kJ��֪��ϵ��n(NO2)��ʱ��仯���±���
2N2O5(g)+5286 kJ��֪��ϵ��n(NO2)��ʱ��仯���±���
| t(s) | 0 | 500 | 1000 | 1500 |
| n(NO2)(mol) | 20 | 13.96 | 10.08 | 10.08 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
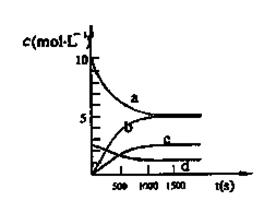
ijС������H2C2O4��Һ������KMnO4��Һ��Ӧ��̽������������Ի�ѧ��Ӧ���ʵ�Ӱ�족��ʵ��ʱ���ȷֱ���ȡ������Һ��Ȼ�����Թ���Ѹ����Ͼ��ȣ���ʼ��ʱ��ͨ���ⶨ��ɫ����ʱ�����жϷ�Ӧ�Ŀ�������С����������·�����
| ʵ���� | H2C2O4��Һ | ����KMnO4��Һ | �¶� | ||
| Ũ��(mol·L��1) | ���(mL) | Ũ��(mol·L��1) | ��� (mL) | ||
| �� | 0.10 | 2.0 | 0.010 | 4.0 | 25 |
| �� | 0.20 | 2.0 | 0.010 | 4.0 | 25 |
| �� | 0.20 | 2.0 | 0.010 | 4.0 | 50 |
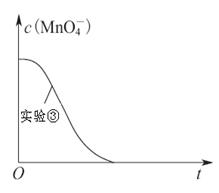
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��֪��ӦA��g��+B(g) C(g)+D(g)��H��0�ش��������⣺
C(g)+D(g)��H��0�ش��������⣺
��1���÷�Ӧ��________��Ӧ������ȡ����ȡ���
��2������Ӧ�ﵽƽ��ʱ�������¶ȣ�A��ת����________���������С�����䡱����ԭ����________________________________________��
��3����Ӧ��ϵ�м���������Է�Ӧ���Ƿ���Ӱ�죿________��ԭ����_________________________________________________��
��4����Ӧ��ϵ�м����������Ӧ����________���������С�����䡱������Ӧ�Ļ��________���������С�����䡱����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
ij�¶�ʱ����һ���ݻ�Ϊ2 L���ܱ������У�X��Y��Z���������ʵ����ʵ�����ʱ��ı仯������ͼ��ʾ������ͼ�����ݣ�����д���пհף�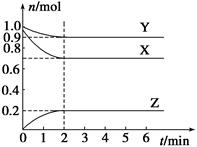
��1���÷�Ӧ�Ļ�ѧ����ʽΪ_______________��
��2����Ӧ��ʼ��2 min������Z�ķ�Ӧ����Ϊ____________��
��3����X��Y��Z��Ϊ���壬��Ӧ�ﵽƽ��ʱ��
��ѹǿ�ǿ�ʼʱ��________����
������ʱ�������������СΪԭ���� 0.5�����ﵽƽ��ʱ���������¶Ƚ�����(���������������Ƚ���)����÷�Ӧ������ӦΪ________��Ӧ(����ȡ������ȡ�)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�����Ϊ10L�������У�ͨ��һ������CO��H2O����850��ʱ�������·�Ӧ��
CO(g)ʮH2O(g)  CO2(g)ʮH2 (g) ��H<0 �� CO��H2OŨ�ȱ仯����ͼ��
CO2(g)ʮH2 (g) ��H<0 �� CO��H2OŨ�ȱ仯����ͼ��
��1) 3min��4min֮�䷴Ӧ����____״̬����ƽ�⡢��ƽ�⣩��
��2��Ҫʹ��Ӧ��8min��ƽ�����淽���ƶ����ɲ�ȡ�Ĵ�ʩ��__ ___��Ҫʹ��Ӧ��8min��Ӧ���ʽ��ͣ�ƽ�����������ƶ����ɲ�ȡ�Ĵ�ʩ��________������a,b,c,d��
a������ˮ���� b�������¶� c��ʹ�ô��� d����������Ũ��
��3�����850�� ʱ���÷�Ӧ��ƽ�ⳣ����CO��ƽ��ת���ʣ�д����ϸ������̣�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��7�֣��ϳ�������Ҫ�ɷ���һ����̼�������������ںϳɶ����ѵ����ȼ�ϣ�����Ȼ����úϳ��������п��ܷ����ķ�Ӧ�У�
��CH4��g��+H2O��g��?CO��g��+3H2��g����H1=+206��1kJ/mol
��CH4��g��+CO2��g��?2CO��g��+2H2��g����H2=+247��3kJ/mol
��CO��g��+H2O��g��?CO2��g��+H2��g����H3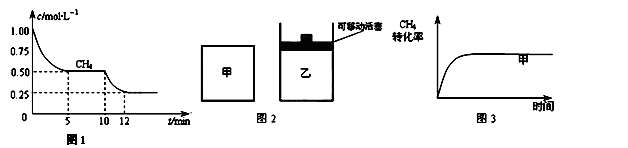
��ش��������⣺
��1����һ�����ܱ������н��з�Ӧ�٣����CH4�����ʵ���Ũ���淴Ӧʱ��ı仯��ͼ1��ʾ����Ӧ���е�ǰ5min�ڣ� ��H2��= ��10minʱ���ı��������������� ��
��H2��= ��10minʱ���ı��������������� ��
��2����ͼ2��ʾ���ڼס����������зֱ��������ʵ�����CH4��CO2��ʹ�ס�����������ʼ�ݻ���ȣ�����ͬ�¶��·�����Ӧ�ڣ���ά�ַ�Ӧ�������¶Ȳ��䣮��֪��������CH4��ת������ʱ��仯��ͼ����ͼ3��ʾ������ͼ3�л�����������CH4��ת������ʱ��仯��ͼ��
��3����Ӧ���С�H3= ��800��ʱ����Ӧ�۵Ļ�ѧƽ�ⳣ��K=1��0��ijʱ�̲�ø��¶��µ��ܱ������и����ʵ����ʵ������±���
| CO | H2O | CO2 | H2 |
| 0��5mol | 8��5mol | 2��0mol | 2��0mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�״�����Ҫ�Ļ�ѧ��ҵ����ԭ�Ϻ����Һ��ȼ�ϡ���ҵ�Ͽ�����CO��CO2������ȼ�ϼ״�����֪�״��Ʊ����йػ�ѧ��Ӧ�Լ��ڲ�ͬ�¶��µĻ�ѧ��Ӧƽ�ⳣ�����±���ʾ��
| ��ѧ��Ӧ | ƽ�ⳣ�� | �¶ȡ� | |
| 500 | 800 | ||
��2H2(g)+CO(g) CH3OH(g) CH3OH(g) | K1 | 2.5 | 0.15 |
��H2(g)+CO2(g) H2O (g)+CO(g) H2O (g)+CO(g) | K2 | 1.0 | 2.50 |
��3H2(g)+CO2(g) CH3OH(g)+H2O (g) CH3OH(g)+H2O (g) | K3 | | |
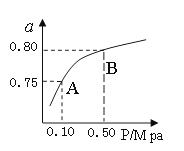


�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��1���������������������£��о��ı���ʼ�������ʵ�������n��H2����ʾ�ݶ�N2(g)��3H2(g) 2NH3(g)��Ӧ��Ӱ�죬ʵ�����ɱ�ʾ����ͼ��ʾ�Ĺ��ɣ�ͼ��T��ʾ�¶ȣ�n��ʾ���ʵ�������
2NH3(g)��Ӧ��Ӱ�죬ʵ�����ɱ�ʾ����ͼ��ʾ�Ĺ��ɣ�ͼ��T��ʾ�¶ȣ�n��ʾ���ʵ�������

�ٱȽ���a��b��c����������ƽ��״̬�У���Ӧ��N2��ת������ߵ���__________��
���������ݻ�Ϊ1L��n��3mol����Ӧ�ﵽƽ��ʱN2��H2��ת���ʾ�Ϊ60%��������ʼʱ��ϵ�м���N2�����ʵ���Ϊ__________mol���������£�T2������Ӧ��ƽ�ⳣ��K��_________�����¶�����ʱ��ƽ�ⳣ����__________��
��ͼ����T2��T1�Ĺ�ϵ��__________��������ڡ��������ڡ��������ڡ�������ȷ��������[ .Com]
��2��������������145��Ϳ�ʼ��Ӧ���ڲ�ͬ�¶Ⱥʹ������������ɲ�ͬ�����ͼ����
4NH3��5O2 4NO��6H2O ��4NH3��3O2
4NO��6H2O ��4NH3��3O2 2N2��6H2O
2N2��6H2O
�¶Ƚϵ�ʱ������__________Ϊ�����¶ȸ���900��ʱ��NO�����½���ԭ����___________________
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com