
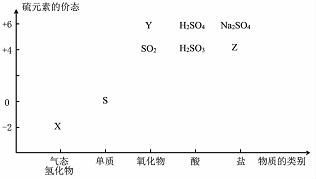
 物质的类别和核心元素的化合价是研究物质性质的两个基本视角?
物质的类别和核心元素的化合价是研究物质性质的两个基本视角?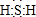 ;其水溶液长期在空气中放置容易变浑浊,该变化体现出:S非金属性比O弱 (填“强”或“弱”)?用原子结构解释原因:同主族元素最外层电子数相同,从上到下,电子层数增多,原子半径增大,得电子能力逐渐减弱?
;其水溶液长期在空气中放置容易变浑浊,该变化体现出:S非金属性比O弱 (填“强”或“弱”)?用原子结构解释原因:同主族元素最外层电子数相同,从上到下,电子层数增多,原子半径增大,得电子能力逐渐减弱?| 溶解度(s)/g | 溶度积(Ksp) | ||
| Ca(OH)2 | Ba(OH)2 | CaCO3 | BaCO3 |
| 0.16 | 3.89 | 2.9×10-9 | 2.6×10-9 |
分析 (1)X为H2S,S最外层6个电子,能够与2个H原子形成共价键;H2S在空气中变浑浊是因为被氧气氧化为S;同主族元素最外层电子数相同,原子半径自上而下逐渐增大,得电子能力逐渐减弱,失电子能力逐渐增强;
(2)①Na2S2O3中S为+2价,从氧化还原的角度分析,反应物中S元素化合价必须分别大于2和小于2;
②硫代硫酸钠与稀硫酸反应生成了单质硫,溶液变浑浊,反应速率越快,出现浑浊时间越短;
(3)①由信息可知转化为单质S和无毒的气体二氧化碳,利用已知热化学方程式,利用盖斯定律可知①×2-②得到2CO(g)+SO2 (g)═S(s)+2CO2(g);
②反应达到平衡状态时正逆反应速率相等,各组分浓度保持不变;利用三段式法得到平衡的各物质浓度,由达平衡时混合气体中CO的体积分数为$\frac{7}{11}$计算转化的量,再计算二氧化硫的转化率;
(4)甲醇作燃料电池,以氢氧化钾为电解质,则负极上甲醇失去电子生成碳酸根离子;
(5)由表格数据可知,溶度积相差不大,但溶解度差异大,溶解度大的其浓度大,吸收效果好.
解答 解:(1)X中S元素的化合价为-2价,则X为H2S,S最外层6个电子,能够与2个H原子形成共价键,其电子式为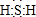 ;H2S在空气中变浑浊是因为被氧气氧化为S,所以S非金属性比O弱;同主族元素最外层电子数相同,原子半径自上而下逐渐增大,得电子能力逐渐减弱,失电子能力逐渐增强,
;H2S在空气中变浑浊是因为被氧气氧化为S,所以S非金属性比O弱;同主族元素最外层电子数相同,原子半径自上而下逐渐增大,得电子能力逐渐减弱,失电子能力逐渐增强,
故答案为: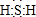 ;弱;电子层数增多,原子半径增大;
;弱;电子层数增多,原子半径增大;
(2)①Na2S2O3中S为+2价,从氧化还原的角度分析,反应物中S元素化合价必须分别大于2和小于2,a中S化合价都小于2,c中S的化合价都大于2,bd符合题意,
故答案为:bd;
②根据硫代硫酸钠与稀硫酸反应生成了单质硫,溶液变浑浊,可以判断反应速率快慢,反应速率越快,出现浑浊时间越短,故答案为:b;
(3)①已知:①CO(g)+$\frac{1}{2}$O2(g)=CO2(g)△H=-283kJ•mol-1
②S(s)+O2(g)=SO2(g)△H=-296kJ•mol-1
由盖斯定律可知①×2-②得到2CO(g)+SO2 (g)═S(s)+2CO2(g)△H=-270 kJ•mol-1,
故答案为:2CO(g)+SO2 (g)═S(s)+2CO2(g)△H=-270 kJ•mol-1;
②a.CO和SO2的速率之比始终等于化学计量数之比,其无法判断反应是否达到平衡状态,故a错误;
b.温度不变平衡常数始终不变,平衡常数不变不能说明反应达到平衡状态,故b错误;
c.容器体积不变,S为固态,反应正向进行气体体积减小,当气体质量不变时,说明各组分浓度不变,反应达到平衡状态,故c正确;
d.CO2和SO2的体积比保持不变说明正逆反应速率相等,反应达到平衡状态,故d正确;
由 2CO(g)+SO2 (g)═S(s)+2CO2(g)
反应前(mol) 4 1 0 0
转化了(mol)2x x x 2x
平衡后(mol)4-2x 1-x x 2x
混合气体中CO的体积分数为$\frac{7}{11}$,则有$\frac{4-2x}{4-2x+1-x+2x}$=$\frac{7}{11}$,解得x=0.6,
所以SO2的转化率为$\frac{0.6}{1}$×100%=60%,
故答案为:cd;60%;
(4)甲醇燃料电池以氢氧化钾为电解质,则负极上甲醇失去电子生成碳酸根离子,负极反应为CH3OH-6e-+8OH-=CO32-+6H2O,故答案为:CH3OH-6e-+8OH-=CO32-+6H2O;
(5)由表格数据可知,碳酸钙、碳酸钡的溶度积相差不大,但Ca(OH)2、Ba(OH)2溶解度差异大,溶解度大的其浓度大,吸收效果好,则吸收CO2最合适的试剂是Ba(OH)2溶液,故答案为:Ba(OH)2.
点评 本题考查较综合,涉及氧化还原反应、元素周期律的应用、化学平衡计算、盖斯定律应用、电极反应及图象、表格数据分析等,注重高频考点的考查,把握反应原理、信息处理及应用为解答的关键,综合性较强,题目难度中等.


 浙江之星学业水平测试系列答案
浙江之星学业水平测试系列答案 高效智能课时作业系列答案
高效智能课时作业系列答案科目:高中化学 来源: 题型:解答题
| 实验编号 | 反应物 | 催化剂 |
| ① | 10mL 2% H2O2溶液 | 无 |
| ② | 10mL 5% H2O2溶液 | 无 |
| ③ | 10mL 5% H2O2溶液 | 1mL 0.1mol•L-1 FeCl3溶液 |
| ④ | 10mL 5% H2O2溶液+少量HCl溶液 | 1mL 0.1mol•L-1 FeCl3溶液 |
| ⑤ | 10mL 5% H2O2溶液+少量NaOH溶液 | 1mL 0.1mol•L-1 FeCl3溶液 |

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | W、X两元素对应的单质发生反应只能得到W2X | |
| B. | 由X、Y、Z三种元素组成的物质其水溶液一定呈中性 | |
| C. | 1 mol Z2X2与足量水反应可得气体11.2 L | |
| D. | 四种元素在自然界中均以化合态存在 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
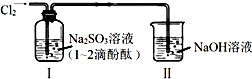
| A. | 通入Cl2后,装置Ⅰ中发生了氧化还原反应 | |
| B. | Cl2与Na2SO3溶液反应的离子方程式是:SO32-+Cl2+H2O=SO42-+2Cl-+2H+ | |
| C. | 通入Cl2后,装置Ⅰ中溶液不褪色 | |
| D. | 装置Ⅱ的作用是吸收尾气,防止污染空气 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 每个四氢大麻酚分子中含有3个手性碳原子 | |
| B. | 四氢大麻酚能与FeCl3溶液发生显色反应 | |
| C. | 1mol四氢大麻酚最多可与1molBr2发生加成反应 | |
| D. | 1mol四氢大麻酚与NaOH溶液反应,最多消耗2molNaOH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 Hg是水体污染的重金属元素之一.水溶液中二价汞的主要存在形态与C1-、OH-的浓度关系如图所示[图中的物质或粒子只有Hg(OH)2为难溶物;pCl=-lgc(Cl-)].下列说法不正确的是( )
Hg是水体污染的重金属元素之一.水溶液中二价汞的主要存在形态与C1-、OH-的浓度关系如图所示[图中的物质或粒子只有Hg(OH)2为难溶物;pCl=-lgc(Cl-)].下列说法不正确的是( )| A. | 可用如下方法除去污水中的Hg2+:FeS(s)+Hg2+(aq)=HgS(s)+Fe2+(aq) | |
| B. | 当溶液pCl保持在1,pH在6~8时,汞元素主要以HgCl42-形式存在 | |
| C. | HgCl2是一种强电解质,其电离方程式是:HgCl2=HgCl++Cl- | |
| D. | 当溶液pH保持在5,pCl由2改变至6时.可使HgCl2转化为Hg(OH)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 乙:
乙:
| 分子式 | C9H8O |
| 部分性质 | 能使Br2CCl4褪色 |
 $→_{Ⅱ}^{一定条件}$Y$→_{Ⅲ}^{一定条件}$乙
$→_{Ⅱ}^{一定条件}$Y$→_{Ⅲ}^{一定条件}$乙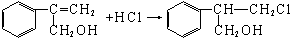 (不需注明反应条件).
(不需注明反应条件).
 .
. 、
、 、
、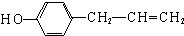 任意一种.
任意一种.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
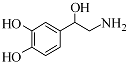
| A. | 每个去甲肾上腺素分子中含有3个酚羟基 | |
| B. | 每个去甲肾上腺素分子中含有2个手性碳原子 | |
| C. | 1mol去甲肾上腺素最多能与2molBr2发生取代反应 | |
| D. | 去甲肾上腺素既能与盐酸反应,又能与氢氧化钠溶液反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com