
| A£® | ·Ö½ā·“Ó¦²»Ņ»¶ØŹĒŃõ»Æ»¹Ō·“Ó¦ | |
| B£® | ·Ē½šŹōµ„ÖŹŌŚ»Æѧ·“Ó¦ÖŠÖ»×öŃõ»Æ¼Į | |
| C£® | ijĪļÖŹ±»»¹ŌŹ±£¬øĆŌŖĖŲŅ»¶Ø“Ó»ÆŗĻĢ¬±äĪŖÓĪĄėĢ¬ | |
| D£® | Ńõ»Æ¼Į±»Ńõ»Æ£¬»¹Ō¼Į±»»¹Ō |
·ÖĪö Ńõ»Æ»¹Ō·“Ó¦ÖŠ“ęŌŚŌŖĖŲ»ÆŗĻ¼Ū±ä»Æ£¬Ńõ»Æ¼ĮµĆµē×Ó±»»¹Ō£¬»¹Ō¼ĮŹ§µē×Ó±»Ńõ»Æ£¬ŅŌ“ĖĄ“½ā“š£®
½ā“š ½ā£ŗA£®·Ö½ā·“Ó¦ÖŠ²»Ņ»¶Ø“ęŌŚ»ÆŗĻ¼ŪµÄ±ä»Æ£¬ĖłŅŌ·Ö½ā·“Ó¦²»Ņ»¶ØŹĒŃõ»Æ»¹Ō·“Ó¦£¬ČēĀČ»Æļ§µÄ·Ö½ā·“Ó¦ŹōÓŚ·ĒŃõ»Æ»¹Ō·“Ó¦£¬¹ŹAÕżČ·£»
B£®·Ē½šŹōµ„ÖŹŌŚ»Æѧ·“Ó¦ÖŠČōŹ§µē×Ó£¬ŌņĪŖ»¹Ō¼Į£¬ČēĒāĘųÓėĀČĘų·“Ó¦Ź±£¬ĒāĘųĪŖ»¹Ō¼Į£¬¹ŹB“ķĪó£»
C£®Ä³ĪļÖŹ±»»¹ŌŹ±£¬øĆŌŖĖŲ»ÆŗĻ¼ŪŅ»¶Ø½µµĶ£¬µ«ŹĒ²»Ņ»¶Ø½µµĶµ½0¼Ū£¬ČēĢśĄė×ÓÓėCu·“Ó¦£¬ĢśĄė×Ó±»»¹ŌĪŖŃĒĢśĄė×Ó£¬¹ŹC“ķĪó£»
D£®Ńõ»Æ¼ĮµĆµē×Ó±»»¹Ō£¬»¹Ō¼ĮŹ§µē×Ó±»Ńõ»Æ£¬¹ŹD“ķĪó£»
¹ŹŃ”A£®
µćĘĄ ±¾Ģāæ¼²éŃõ»Æ»¹Ō·“Ó¦£¬°ŃĪÕ·“Ó¦ÖŠŌŖĖŲµÄ»ÆŗĻ¼Ū±ä»ÆĪŖ½ā“šµÄ¹Ų¼ü£¬²ąÖŲŃõ»Æ»¹Ō·“Ó¦»ł±¾øÅÄīµÄ漲飬ĢāÄæÄŃ¶Č²»“ó£®


 ŠĒ¼¶æŚĖćĢģĢģĮ·ĻµĮŠ“š°ø
ŠĒ¼¶æŚĖćĢģĢģĮ·ĻµĮŠ“š°ø Ć¢¹ū½ĢøØ“ļ±ź²āŹŌ¾ķĻµĮŠ“š°ø
Ć¢¹ū½ĢøØ“ļ±ź²āŹŌ¾ķĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
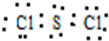 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | øßŃ¹ÓŠĄūÓŚ°±µÄŗĻ³É | |
| B£® | Ļņŗ¬ÓŠ·ÓĢŖµÄ°±Ė®ČÜŅŗÖŠ£¬¼ÓČėÉŁĮæNH4Cl¾§Ģ壬ČÜŅŗŗģÉ«±äĒ³ | |
| C£® | ³£ĪĀĻĀ£¬0.1 mol•L-1µÄŃĪĖįÖŠ£¬ÓÉĖ®²śÉśµÄc£ØH+£©£¼1.0”Į10-7mol•L-1 | |
| D£® | Ź¹ÓĆ“ß»Æ¼ĮæɼÓæģSO2×Ŗ»ÆĪŖSO3µÄ·“Ó¦ĖŁĀŹ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ·ŹŌķŗĶŗĻ³ÉĻ“µÓ¼ĮµÄ½į¹¹ĻąĖĘ£¬¶¼ŗ¬ÓŠŌ÷Ė®»łŗĶĒ×Ė®»ł | |
| B£® | ·ŹŌķ²»ŹŹÓĆÓŚÓ²Ė®ÖŠĻ“µÓ£¬ŗĻ³ÉĻ“µÓ¼ĮæÉŅŌ | |
| C£® | ŗĻ³ÉĻ“µÓ¼ĮÄŃŅŌ±»Ī¢ÉśĪļ·Ö½ā£¬ĖłŅŌČ„ĪŪÄÜĮ¦±Č·ŹŌķŗĆ | |
| D£® | ·ŹŌķµÄÉś²śŌĮĻŹĒÓĶÖ¬£¬³É±¾øߣ¬ŗĻ³ÉĻ“µÓ¼ĮµÄÉś²śŌĮĻŹĒŹÆÓĶø±²śĘ·£¬³É±¾½ĻµĶ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĶʶĻĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | æĢ¶ČĻß | B£® | Ź¹ÓĆĪĀ¶Č | C£® | ¹ęøń | D£® | 0æĢ¶Č |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com