
| A. | 氯气溶于水:Cl2+H2O═2H++Cl-+ClO- | |
| B. | 明矾溶于水产生Al(OH)3胶体:Al3++3H2O═Al(OH)3↓+3H+ | |
| C. | Na2O2溶于水产生O2:Na2O2+H2O═2Na++2OH-+O2↑ | |
| D. | Ca(HCO3)2溶液与少量NaOH溶液反应:HCO3-+Ca2++OH-═CaCO3↓+H2O |
分析 A.次氯酸为弱酸,离子方程式中次氯酸不能拆开;
B.该反应为可逆反应,应该用可逆号,且不能使用沉淀符号;
C.2mol过氧化钠与水反应生成1mol氧气,该反应不满足电子守恒;
D.氢氧化钠少量,离子方程式按照氢氧化钠的化学式组成书写.
解答 解:A.氯气溶于水生成氯化氢和次氯酸,正确的离子方程式为:Cl2+H2O═H++Cl-+HClO,故A错误;
B.明矾溶于水产生Al(OH)3胶体,不能使用沉淀符号,且应该用可逆号,正确的离子方程式为:Al3++3H2O?Al(OH)3+3H+,故B错误;
C.Na2O2溶于水生成氢氧化钠和O2,正确的离子方程式为:2Na2O2+2H2O═4Na++4OH-+O2↑,故C错误;
D.Ca(HCO3)2溶液与少量NaOH溶液反应生成碳酸钙沉淀、碳酸氢钠和水,反应的离子方程式为:HCO3-+Ca2++OH-═CaCO3↓+H2O,故D正确;
故选D.
点评 本题考查了离子方程式的书写判断,题目难度不大,注意掌握离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合守恒关系(如:质量守恒和电荷守恒等)、检查是否符合原化学方程式等.


科目:高中化学 来源: 题型:选择题
| 化学性质 | 实际应用 | |
| A | SiCl4与水反应时生成白色烟雾 | SiCl4在战争中可用作烟雾弹 |
| B | 铁比铜金属性强 | FeCl3腐蚀Cu刻制印刷电路板 |
| C | MgO是一种电解质 | 工业电解冶炼金属镁 |
| D | 铝耐腐蚀 | 用铝质容器研制咸菜 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铝制的容器可以贮存浓硫酸或浓硝酸 | |
| B. | 铝容易形成致密的氧化膜,抗腐蚀性能好 | |
| C. | 工业上电解氯化铝溶液可分解得到铝和氯气 | |
| D. | 工业上常用铝热反应进行焊接铁轨 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.225mol/L | B. | 0.25mol/L | C. | 0.45mol/L | D. | 0.55mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
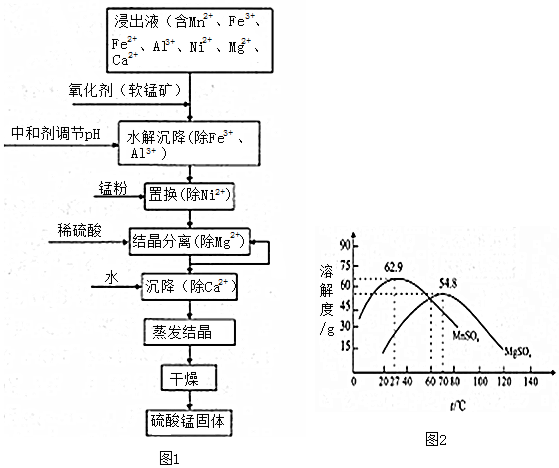
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
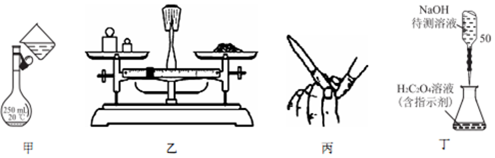
| A. | 用图甲所示操作转移NaOH 溶液到容量瓶中 | |
| B. | 用图乙所示装置准确称得0.1575gH2C2O4•2H2O固体 | |
| C. | 用图丙所示操作检查碱式滴定管是否漏液 | |
| D. | 用图丁所示装置以NaOH 待测液滴定H2C2O4溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
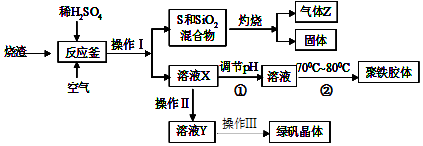
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com