
【题目】下列说法正确的是( )
A.40gNaOH溶于水所得1L溶液的浓度为1mol·L-1
B.1mol·L-1的Na2CO3溶液中Na+的浓度为1mol·L-1
C.从1L0.1mol·L-1的NaCl溶液中取出0.1L溶液,则NaCl的浓度变为0.01 mol·L-1
D.1L0.2 mol·L-1的Na2SO4溶液中,Na+的物质的量为0.2 mol
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】已知25oC时,H2A的Ka1=10-1.85,Ka2=10-7.19。用0.1mol·L-1NaOH溶液滴定20mL0.1mol·L-1H2A溶液的滴定曲线如图所示(曲线上的数字为pH)。下列说法不正确的是
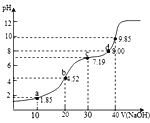
A.a点所得溶液中:2c(H2A)+c(A2-)<0.1mol·L-1
B.NaHA溶液中由水电离出的氢离子浓度小于1.0×10-7mol·L-1
C.c点所得溶液中:c(Na+)<3c(HA_)
D.d点所得溶液中:c(Na+)>c(A2-)>c(HA-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是部分短周期元素的单质及其化合物(或其溶液)的转化关系。已知在常温常压下,A是固体,B、C、D、E是非金属单质且都是气体,C呈黄绿色;化合物F是淡黄色固体,化合物G的焰色反应为黄色,化合物Ⅰ和J通常状况下呈气态;D和E反应生成一种刺激性气味的气体。
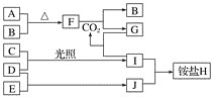
请回答下列问题:
(1)E和J的化学式分别是________和________。
(2)写出F和CO2反应的化学方程式并用单线桥法表示电子转移的情况:_________。
(3)将少量单质C通入盛有淀粉碘化钾溶液的试管中,溶液变蓝色,该反应的离子方程式为_________。
(4)标况下3.36 L气体B与A完全反应,转移电子的数目为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物A含碳72.0%、含氢为6.67%,其余为氧用质谱法分析得知A的相对分子质量为150,A在光照条件下生成一溴代物B,B分子的核磁共振氢谱中有4组峰,峰面积比为2:2:2:3,B可发生如下转化关系(无机产物略):
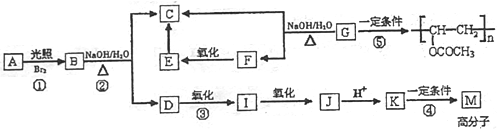
已知:①K与氧化铁溶液发生显色反应,且环上的一元取代物只有两种结构
②当羟基与双键碳原子相连时,会发生如下转化:RCH=CHOH→RCH2CHO
请回答下列问题:
(1)B中官能团的名称是___________,反应④属于______反应类型。
(2)A的结构简式:___________。
(3)F与银氨溶液反应的离子方程式为:__________________。
(4)写出下列反应的化学方程式
反应②:________________。反应④:_______________________。
(5)N是比K多1个碳原子的同系物,同时符合下列要求的N的同分异构体有_____种。
I.苯环上有两个取代基;II.能发生水解反应;III.与氯化铁溶液发生显色反应
其中核磁共振氢谱为5组峰的为_________(写结构简式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在好氧菌和厌氧菌作用下废液中NH4+能转化为N2(g)和H2O(l),示意图如下:
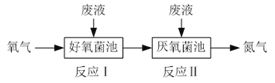
反应I:NH4+(aq)+2O2(g)=NO3-(aq)+2H+(aq)+H2O(l) ΔH1=a kJ·mol-1
反应II:5NH4+(aq)+3NO3-(aq)=4N2(g)+9H2O(l)+2H+(aq) ΔH2=b kJ·mol-1
下列说法正确的是
A. 两池发生的反应中氮元素只被氧化
B. 两池中投放的废液体积相等时NH4+能完全转化为N2
C. 常温常压下,反应II中生成22.4 L N2转移的电子数为3.75×6.02×1023
D. 4NH4+(aq)+3O2(g)=2N2(g)+4H+(aq)+6H2O(l) ΔH=![]() (3a+b) kJ·mol-1
(3a+b) kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某铝合金(硬铝)中含有镁、铜、硅,为了测定该合金中铝的含量,有人设计如下实验:
(1)称取样品ag。
(2)将样品溶于足量稀盐酸中,过滤,滤液中主要含有___离子,滤渣中含有___;在溶解过滤时使用的仪器有___。
(3)往滤液中加入过量NaOH溶液,过滤,写出该步操作中有关的离子方程式____。
(4)在第(3)步的滤液中通入足量CO2过滤,将沉淀用蒸馏水洗涤数次后,烘干并灼烧至质量不再减少为止,冷却后称量,质量为bg。有关反应的化学方程式为____。
(5)计算该样品中铝的质量分数的表达式为___。
(6)若第(3)步中加入NaOH溶液的量不足时,会使测定的结果___(“偏高”“偏低”或“无影响”,下同)。若第(4)步对沉淀的灼烧不充分时,会使测定的结果___。若第(4)步中的沉淀没有用蒸馏水洗涤时,会使测定的结果____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2019年新发现的元素鉝(Lv)是116号主族元素,其原子核外最外层电子数是6。下列说法不正确的是 ( )
A.Lv位于第七周期第VIA族B.Lv在同主族元素中金属性最弱
C.Lv的同位素原子具有相同的电子数D.中子数为177的Lv核素符号为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,W、X、Y、Z为短周期主族元素,Y和Z两元素的原子序数之和等于W元素的原子序数。下列说法错误的是( )
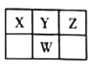
A.X、Y、W分别与Z都能形成两种或两种以上的化合物,这些化合物都能与NaOH反应
B.X、Y、Z都能形成10、18 电子的氢化物分子,其中X的最简单氢化物沸点最低
C.Y、Z、W与氢四种元素能组成离子化合物,该化合物能发生水解
D.最高价氧化物对应水化物的酸性:Y>W>X
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】产自我国西北某盐湖的“块碱”是一种Na2CO3和NaCl的混合物。可通过以下方法对块碱样品的组成和含量进行分析测定。
I.定性测定NaCl的存在:
(1)取样品少许溶于水,加入足量稀硝酸充分反应后再滴加______溶液,能观察到有______________产生,说明块碱中含有NaCl。
II.定量测定Na2CO3的含量:准确称量w g样品置于如图所示的装置中,向其中加入足量稀硫酸,通过测定生成气体的体积来求算Na2CO3的含量。请回答下列相关问题:
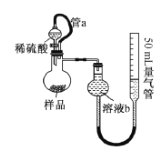
(2)测定装置中,导管a的作用是__________________。
(3)为提高测定的准确度,溶液b最宜选用__________________。
①饱和食盐水 ②饱和NaHCO3溶液 ③澄清石灰水 ④酸性KMnO4溶液
(4)以下是测量收集到气体体积必须包括的几个步骤:①调整橡胶管所连两装置液面高度使之相同;②使装置内的气体都冷却至室温;③读取碱式滴定管的示数。这三步操作的正确顺序是:________(请填写步骤代号)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com