
| A. | ③①④②⑤ | B. | ③①⑤④② | C. | ③②①⑤④ | D. | ⑤②④①③ |
分析 溶液酸性越强,溶液的pH越小,则溶液的pH:酸性<中性<碱性;先将溶液分为酸性、中性和碱性,然后根据电离程度、盐的水解情况判断各溶液的pH大小.
解答 解:①(NH4)2SO4、④NH4NO3水解呈酸性,两溶液的pH<7;③NH4HSO4电离出H+呈酸性,pH<7;
②NaNO3不水解,其pH=7;
⑤CH3COONa水解呈碱性,pH>7,
①、④比较,前者c(NH4+)大,水解生成c(H+)大,pH小,①③比较,后者电离出c(H+)比前者水解出c(H+)大,pH小,
所以溶液的pH从小到大的顺序为:③①④②⑤,
故选A.
点评 本题考查溶液pH的大小比较,题目难度不大,要考虑盐类的水解程度大小,注意硫酸氢铵中硫酸氢根离子电离出氢离子,试题培养了学生的灵活应用基础知识的能力.


科目:高中化学 来源: 题型:选择题
| A. | 等于10s | B. | 等于5 s | C. | 大于10 s | D. | 小于10 s |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
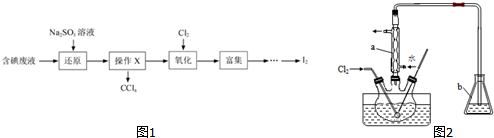
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
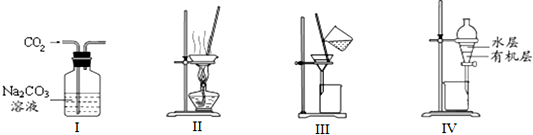
| A. | 用图I除去CO2中含有的少量Cl2 | |
| B. | 用图Ⅱ蒸干NH4Cl饱和溶液制备NH4Cl晶体 | |
| C. | 用图Ⅲ分离NaCl和Na2SO4的混合溶液 | |
| D. | 用图Ⅳ分离CCl4萃取碘水中的碘后已分层的有机层和水层 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 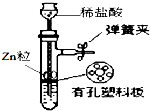 用如图所示装置制取少量H2 | |
| B. | 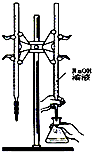 用如图所示装置用标准浓度的氢氧化钠溶液测定盐酸的浓度 | |
| C. | 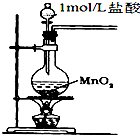 用如图所示装置制取少量Cl2 | |
| D. | 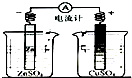 用如图所示装置确定导线中有电流通过及并确定电流方向 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 先滴加氯水,再滴加KSCN溶液后显红色 | |
| B. | 先滴加KSCN溶液,不显红色,再滴加氯水后显红色 | |
| C. | 滴加NaOH溶液,产生灰绿色沉淀,最后呈红褐色 | |
| D. | 只需滴加KSCN溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
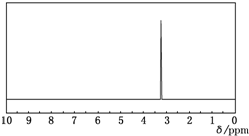
| A. | CH3CH2OH | B. | CH3CH2CH2OH | C. | CH3-O-CH3 | D. | CH3CHO |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
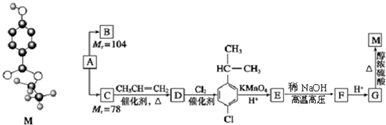
 .
.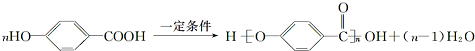 .
.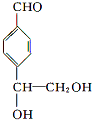 等.
等.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com