

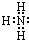 ,故答案为:
,故答案为: ;
; Si3N4+12HCl,故答案为:3SiCl4+4NH3
Si3N4+12HCl,故答案为:3SiCl4+4NH3 Si3N4+12HCl;
Si3N4+12HCl; 2CO+Si,属于置换反应,故a正确;
2CO+Si,属于置换反应,故a正确;

 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案科目:高中化学 来源: 题型:
| 元素 | 结构特点及在周期表中的位置 | 单质及化合物的都分性质与用途 |
| 甲 | 在元素周期表中,主族序数等于周期数 | 工业上用电解法冶炼该金属 |
| 乙 | 单质的晶体类型为原子晶体 | 氧化物是工业制普通玻璃的主要原料 |
| 丙 | 原子最外层电子数是最内层电子数的2倍 | 单质存在多种同素异形体 |
| 丁 | 元素能形成两种不同的阴离子 | 丁的一种单质与KI溶液反应生成另一种丁的单质 |
| A、甲、乙、丙、丁 |
| B、丁、甲、乙、丙 |
| C、丙、丁、甲、乙 |
| D、乙、甲、丁、丙 |
查看答案和解析>>
科目:高中化学 来源: 题型:
现有四种短周期元素的有关信息如下表所示:
| 元素 | 结构特点及在周期表中的位置 | 单质及化合物的部分性质与用途 |
| 甲 | 在元素周期表中,主族序数等于周期数 | 工业上用电解法冶炼该金属 |
| 乙 | 单质的晶体类型为原子晶体 | 氧化物是工业制普通玻璃的主要原料 |
| 丙 | 原子最外层电子数是最内层电子数的2倍 | 单质存在多种同素异形体 |
| 丁 | 元素能形成两种不同的阴离子 | 丁的一种单质与KI溶液反应生成另一种丁的单质 |
则甲、乙、丙、丁四种元素的原子序数从大到小排列的是 ( )
A.甲、乙、丙、丁 B.丁、甲、乙、丙
C.丙、丁、甲、乙 D.乙、甲、丁、丙
查看答案和解析>>
科目:高中化学 来源:2012-2013学年广东省执信中学高二下学期期末考试化学试卷(带解析) 题型:实验题
阿司匹林可由水杨酸与乙酸酐作用制得。其制备原理如下:
主反应: +化合物A
+化合物A
水杨酸 乙酸酐 阿司匹林(乙酰水杨酸)
副反应:
聚水杨酸
已知:① 水杨酸可溶于水,乙酰水杨酸的钠盐易溶于水,聚水杨酸(固体)难溶于水;
② 阿司匹林,白色针状或板状结晶或粉末,微溶于水;阿司匹林可按如下步骤制取和纯化:
步骤1:在干燥的50 mL圆底烧瓶中加入2 g水杨酸、5 mL乙酸酐和5滴浓硫酸,振荡使水杨酸全部溶解;
步骤2:按图所示装置装配好仪器,通水,在水浴上加热5~10min,用电炉控制温度在85~90℃;
步骤3:反应结束后,取下反应瓶,冷却,再放入冰水中冷却、结晶、过滤、冷水洗涤2~3次,继续过滤得粗产物;
步骤4:将粗产物转移至150 mL烧杯中,在搅拌下加入25 mL饱和碳酸氢钠溶液,充分搅拌,然后过滤;
步骤5:将滤液倒入10 mL 4 mol/L盐酸溶液,搅拌,将烧杯置于冰浴中冷却,使结晶完全。过滤,再用冷水洗涤2~3次。
(1) 主反应中,生成物中化合物A是____________;
(2) 步骤2组装仪器还需要一种玻璃仪器,名称是________,该仪器的位置如何摆放?____________________________;冷凝管的作用是_________,冷凝管通水,水应从______(填“a”或“b”)口进。
(3) 步骤4过滤得到的固体为________;
(4) 经过步骤5得到产物,发生反应的化学方程式为______________________;
(5) 最后得到的阿司匹林可能会有少量未反应的水杨酸。如何用实验的方法检验步骤5中得到的晶体是否含有水杨酸?___________________________________。若阿司匹林晶体含有水杨酸,还需要采用________方法,进一步纯化晶体。
查看答案和解析>>
科目:高中化学 来源:2014届广东省高二下学期期末考试化学试卷(解析版) 题型:实验题
阿司匹林可由水杨酸与乙酸酐作用制得。其制备原理如下:
主反应: +化合物A
+化合物A
水杨酸 乙酸酐 阿司匹林(乙酰水杨酸)
副反应:
聚水杨酸
已知:① 水杨酸可溶于水,乙酰水杨酸的钠盐易溶于水,聚水杨酸(固体)难溶于水;
② 阿司匹林,白色针状或板状结晶或粉末,微溶于水;阿司匹林可按如下步骤制取和纯化:
步骤1:在干燥的50 mL圆底烧瓶中加入2 g水杨酸、5 mL乙酸酐和5滴浓硫酸,振荡使水杨酸全部溶解;
步骤2:按图所示装置装配好仪器,通水,在水浴上加热5~10min,用电炉控制温度在85~90℃;

步骤3:反应结束后,取下反应瓶,冷却,再放入冰水中冷却、结晶、过滤、冷水洗涤2~3次,继续过滤得粗产物;
步骤4:将粗产物转移至150 mL烧杯中,在搅拌下加入25 mL饱和碳酸氢钠溶液,充分搅拌,然后过滤;
步骤5:将滤液倒入10 mL 4 mol/L盐酸溶液,搅拌,将烧杯置于冰浴中冷却,使结晶完全。过滤,再用冷水洗涤2~3次。
(1) 主反应中,生成物中化合物A是____________;
(2) 步骤2组装仪器还需要一种玻璃仪器,名称是________,该仪器的位置如何摆放?____________________________;冷凝管的作用是_________,冷凝管通水,水应从______(填“a”或“b”)口进。
(3) 步骤4过滤得到的固体为________;
(4) 经过步骤5得到产物,发生反应的化学方程式为______________________;
(5) 最后得到的阿司匹林可能会有少量未反应的水杨酸。如何用实验的方法检验步骤5中得到的晶体是否含有水杨酸?___________________________________。若阿司匹林晶体含有水杨酸,还需要采用________方法,进一步纯化晶体。
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
阿司匹林可由水杨酸与乙酸酐作用制得。其制备原理如下:
主反应: +化合物A
+化合物A
水杨酸 乙酸酐 阿司匹林(乙酰水杨酸)
副反应:
聚水杨酸
已知:① 水杨酸可溶于水,乙酰水杨酸的钠盐易溶于水,聚水杨酸(固体)难溶于水;
② 阿司匹林,白色针状或板状结晶或粉末,微溶于水;
阿司匹林可按如下步骤制取和纯化:
 步骤1:在干燥的50 mL圆底烧瓶中加入2 g水杨酸、5 mL乙酸酐和5滴浓硫酸,振荡使水杨酸全部溶解;
步骤1:在干燥的50 mL圆底烧瓶中加入2 g水杨酸、5 mL乙酸酐和5滴浓硫酸,振荡使水杨酸全部溶解;
步骤2:按图所示装置装配好仪器,通水,在水浴上加热5~10min,
用电炉控制温度在85~90℃;
步骤3:反应结束后,取下反应瓶,冷却,再放入冰水中冷却、结晶、
过滤、冷水洗涤2~3次,继续过滤得粗产物;
步骤4:将粗产物转移至150 mL烧杯中,在搅拌下加入25 mL饱和碳酸氢钠溶液,充分搅拌,然后过滤;
步骤5:将滤液倒入10 mL 4 mol/L盐酸溶液,搅拌,将烧杯置于冰浴中冷却,使结晶完全。过滤,再用冷水洗涤2~3次。
(1) 主反应中,生成物中化合物A是____________;
(2) 步骤2组装仪器还需要一种玻璃仪器,名称是________,该仪器的位置如何摆放?____________________________;冷凝管的作用是_________,冷凝管通水,水应从______(填“a”或“b”)口进。
(3) 步骤4过滤得到的固体为________;
(4) 经过步骤5得到产物,发生反应的化学方程式为______________________;
(5) 最后得到的阿司匹林可能会有少量未反应的水杨酸。如何用实验的方法检验步骤5中得到的晶体是否含有水杨酸?___________________________________。若阿司匹林晶体含有水杨酸,还需要采用________方法,进一步纯化晶体。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com