
【题目】下列各组中的离子,能在溶液中大量共存的是
A. H+、Na+、CO32- B. Cl-、Ba2+、SO42-
C. H+、OH-、SO42- D. H+、Ag+、NO3-
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】在“石蜡 →石蜡油 →石蜡气体→裂化气”的变化过程中,被破坏的作用力依次是()
A.范德华力、范德华力、范德华力B.共价键、共价键、共价键
C.范德华力、共价键、共价键D.范德华力、范德华力、共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用化学方程式解释下列问题:
(1)实验室不用石英坩埚熔化NaOH固体: _________。
(2)漂白粉露置于空气中较长时间后失效: _________。
(3)Fe(OH)2暴露在空气中最后变成红褐色固体: _________。
(4)等物质的量的SO2与Cl2同时通入水中,溶液无漂白性:_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮的化合物在生产生活中广泛存在.
(1)处理生活污水中的NH4+ , 过程如图1: 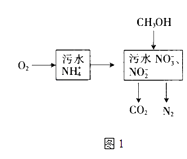
①根据较新的研究表明,将只含NO2﹣的污水与含NH4+的污水按比例混合,直接转化为无毒气体,该气体为 .
②空气将NH4+转变为NO3﹣或NO2﹣ , 溶液pH(填“增大”、“减小”或“不变”).
③完全处理含1mol NH4+污水,则n(O2)与n(CH3OH)关系式为[用n(O2)与n(CH3OH)表示].
(2)用焦炭还原NO2的反应为:2NO2(g)+2C(s )N2(g)+2CO2(g),在恒温条件下,1mol NO2和足量C发生该反应,测得平衡时NO2和CO2的物质的量浓度与平衡总压的关系如图2所示: 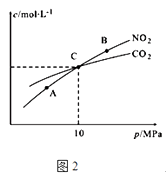
①A、B两点的浓度平衡常数关系:Kc(A)Kc(B) (填“>”、“<”或“﹦”).
②A、B、C三点中NO2的转化率最高的是(填“A”或“B”或“C”)点.
③计算C点时该反应的压强平衡常数Kp(C)=(Kp是用平衡分压代替平衡浓度计算,分压=总压×物质的量分数).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】两种气态烃组成的混和气体0.1mol完全燃烧得0.16摩尔CO2和3.6gH2O,下列说法正确的( )
A. 一定有乙烯B. 一定是甲烷和乙烯
C. 一定有乙炔D. 一定有甲烷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高高纯MnCO3是制备高性能磁性材料的主要原料.实验室以MnO2为原料制备少量高纯MnCO3的操作步骤如下: 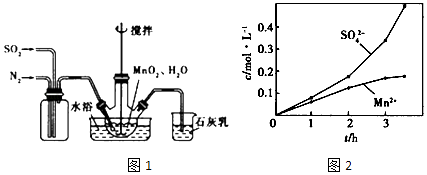
(1)制备MnSO4溶液:在烧瓶中(装置图1)加入一定量MnO2和水,搅拌,通入SO2和N2混合气体,反应3h.停止通入SO2 , 继续反应片刻,过滤
①写出反应方程式:MnO2+H2SO3=;石灰乳参与反应的化学方程式为 .
②反应过程中,为使SO2尽可能转化完全,在通人SO2和N2比例一定、不改变固液投料的条件下,可采取的合理措施有(填两种)、 .
③若实验中将N2换成空气,测得反应液中Mn2+、SO42﹣的浓度随反应时间t变化如图2.导致溶液中Mn2+、SO42﹣浓度变化产生明显差异,若其中Mn2+对O2与H2SO3反应所起的作用是 .
(2)制备高纯MnCO3固体:已知MnCO3难溶于水、乙醇,潮湿时易被空气氧化,100℃开始分解;Mn(OH)2开始沉淀的pH=7.7.
请补充由(1)制得的MnSO4溶液制备高纯MnCO3的操作步骤[实验中可选用的试剂:H2O,Ca(OH)2、NaHCO3、Na2CO3、C2H5OH].
①边搅拌边加入 , 并控制溶液pH7.7;
②;
③;
④;
⑤低于100℃干燥.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】韩梅梅体检的血液化验单中,葡萄糖为6.1 mmol/L,表示该体检指标的物理量是:
A. 质量分数(ω) B. 物质的量(n)
C. 摩尔质量(M) D. 物质的量浓度(c)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:还原性HSO3﹣>I﹣ , 氧化性IO3﹣>I2 . 在含3mol NaHSO3的溶液中逐滴加入KIO3溶液.加入KIO3和析出I2的物质的量的关系曲线如图所示.下列不正确的是( ) 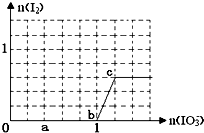
A.0﹣﹣b:3HSO3﹣+IO3﹣=3SO42﹣+I﹣+3H+
B.a点时消耗NaHSO3的物质的量为1.2 mol
C.b﹣c间I2是既是还原产物又是氧化产物
D.当溶液中I与I2的物质的量之比为5:2时,加入的KIO3为1.8mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com