
据新浪网报道,欧洲一集团公司拟在太空建立巨大的激光装置,把太阳光变成激光用于分解海水制氢.有下列几种说法:
①水分解反应是放热反应;
②若用生成的氢气与空气中多余的二氧化碳反应生成甲醇储存起来,可改善生存条件;
③使用氢气作燃料有助于控制温室效应;
④氢气是一级能源.
其中叙述正确的是( )
|
| A. | ①② | B. | ③④ | C. | ②③ | D. | ①②③④ |
| 清洁能源;吸热反应和放热反应. | |
| 分析: | ①水分解反应是吸热反应;②若用生成的氢气与空气中多余的二氧化碳反应生成甲醇储存起来,可以减少二氧化碳的排放量,同时得到新能源甲醇,可改善生存条件;③氢气燃烧只生成水,是洁净的能源;④氢气是二级能源. |
| 解答: | 解:①水分解反应是吸热反应,故①错误; ②若用生成的氢气与空气中多余的二氧化碳反应生成甲醇储存起来,可以减少二氧化碳的排放量,同时得到新能源甲醇,可改善生存条件,故②正确; ③氢气燃烧只生成水,不会生成二氧化碳气体,有助于控制温室效应,故③正确; ④氢气是二级能源,故④错误; 通过以上分析②③正确, 故选C. |
| 点评: | 本题考查了新能源的开发和利用,题目难度不大,解题时抓住新能源的要求﹣节能减排,不难找到答案. |


科目:高中化学 来源: 题型:
在无色透明的强酸性溶液中,能大量共存的是( )
A.Na+、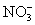 、Al3+、Cl-
、Al3+、Cl-
B.Na+、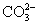 、K+、
、K+、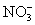
C.Cu2+、K+、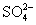 、Cl-
、Cl-
D.Ba2+、K+、Cl-、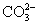
查看答案和解析>>
科目:高中化学 来源: 题型:
298K、10lkPa时,1molH2(g)与O2(g)完全反应生成H2O(g)时放出242kJ热量,而生成H2O(1)时放出286kJ热量,则下列表达不正确的是( )
|
| A. | 2H2(g)+O2(g)=2H2O(g);△H=﹣484kJ•mol﹣1 |
|
| B. | H2O(g)=H2(g)+ |
|
| C. | H2(g)+ |
|
| D. | H2O(1)=H2O(g);△H=﹣44kJ•mol﹣1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
工业合成氨的反应为N2(g)+3H2(g)⇌2NH3(g).设t℃在容积为2L的密闭容器中充入0.6mol N2和1.6mol H2,反应在一定条件下达到平衡时,NH3的物质的量分数为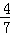 .计算:
.计算:
(1)达到平衡时H2的物质的量;
(2)t℃该反应的平衡常数.
查看答案和解析>>
科目:高中化学 来源: 题型:
在甲、乙两个密闭容器中,发生如下反应:2A(g)  B(g) +2C(s); △H=mkJ ·mol-1。有下列两种图像。下列叙述正确的是( )
B(g) +2C(s); △H=mkJ ·mol-1。有下列两种图像。下列叙述正确的是( )
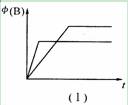

A.若甲为恒容体系,图像(I)代表温度不同时,时间与B的体积分数关系图,则m >0
B.恒温条件下,图像 (I)可能代表压强不同时,时间与B的体积分数关系图
C.恒温条件下,若甲、乙两容器体积相同,起始时分别向甲中充入2 molA,乙中充入1molB、3 molC,则达到平衡后两容器中B的体积分数一定不同
D. 恒温条件下,乙容器存在图像 (II)的关系,则当x代表压强时,y可代表B的体积分数
查看答案和解析>>
科目:高中化学 来源: 题型:
反应 H2(g)+I2(g)⇌2HI(g)的平衡常数K1;反应HI(g)⇌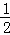 H2(g)+
H2(g)+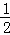 I2(g)的平衡常数K2,则K1、K2的关系为(平衡常数为同温度下的测定值)( )
I2(g)的平衡常数K2,则K1、K2的关系为(平衡常数为同温度下的测定值)( )
|
| A. | K1=2K2 | B. | K1=K22 | C. | K1= | D. | K1= |
查看答案和解析>>
科目:高中化学 来源: 题型:
在一固定体积的密闭容器中,可逆反应,nA(g)+mB (g)⇌pC(g)已经达到平衡状态.已知n+m>p,正反应为放热反应.下列分析结论中正确的是( )
①升温,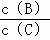 的值变小;
的值变小;
②降温,平衡体系内混合气体的平均相对分子质量变小;
③增加B的物质的量,A的转化率增大;
④使用催化剂,气体总的物质的量不变;
⑤加压使密闭容器的容积变小,A或B的浓度则变大;
⑥若A的反应速率为v(A),则v(B)=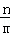 [v(A)].
[v(A)].
|
| A. | ①② | B. | ②③④ | C. | ③④⑤ | D. | ③④⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中正确的是( )
A.二氧化硫溶于水能导电,故二氧化硫属于电解质
B.硫酸钡难溶于水,故硫酸钡属于弱电解质
C.硫酸是强电解质,故纯硫酸能导电
D.氢氧根离子浓度相同的氢氧化钠溶液和氨水导电能力相同
查看答案和解析>>
科目:高中化学 来源: 题型:
配位化学创始人维尔纳发现,将各为1 mol的CoCl3·6NH3(黄色)、CoCl3·5NH3(紫红色)、CoCl3·4NH3(绿色)、CoCl3·4NH3(紫色)四种配合物溶于水,加入足量硝酸银溶液,立即沉淀的氯化银分别为3 mol、2 mol、1 mol、和1 mol。已知上述配合物中配离子的配位数均为6。
(1)请根据实验事实用配合物的形式写出它们的化学式。
CoCl3·6NH3______________________,
CoCl3·5NH3____________________,
CoCl3·4NH3(绿色和紫色)____________。
(2)后两种物质组成相同而颜色不同的原因是它们互为同分异构体,已知绿色的配合物内界结构对称,请在下图中用元素符号标出氯原子的位置。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com