
 (D是
(D是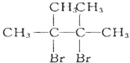 )
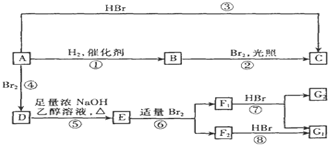
)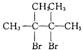 ,则A的结构简式为:(CH3)2C=C(CH3)2;D在氢氧化钠的乙醇溶液中加热生成E,则E为CH2=C(CH3)C(CH3)=CH2;A与氢气发生加成反应生成B,则B为(CH3)2CHCH(CH3)2;A与HBr加成生成C,则C为(CH3)2CHCBr(CH3)2;CH2=C(CH3)C(CH3)=CH2可与溴发生1,2加成或1,4加成,F1与HBr发生加成反应得到G1、G2,且F2与HBr发生加成反应只得到G1,则F2为对称结构,故F1为CH2BrCBr(CH3)C(CH3)=CH2,F2为CH2BrC(CH3)=C(CH3)CH2Br,G1为
,则A的结构简式为:(CH3)2C=C(CH3)2;D在氢氧化钠的乙醇溶液中加热生成E,则E为CH2=C(CH3)C(CH3)=CH2;A与氢气发生加成反应生成B,则B为(CH3)2CHCH(CH3)2;A与HBr加成生成C,则C为(CH3)2CHCBr(CH3)2;CH2=C(CH3)C(CH3)=CH2可与溴发生1,2加成或1,4加成,F1与HBr发生加成反应得到G1、G2,且F2与HBr发生加成反应只得到G1,则F2为对称结构,故F1为CH2BrCBr(CH3)C(CH3)=CH2,F2为CH2BrC(CH3)=C(CH3)CH2Br,G1为 ,G2为CH2BrCBr(CH3)CBr(CH3)CH3,据此分析解答.
,G2为CH2BrCBr(CH3)CBr(CH3)CH3,据此分析解答. ,则A的结构简式为 (CH3)2C=C(CH3)2,
,则A的结构简式为 (CH3)2C=C(CH3)2, ,G2为CH2BrCBr(CH3)CBr(CH3)CH3,
,G2为CH2BrCBr(CH3)CBr(CH3)CH3, ,
, .
.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、体积不变,升温,正反应速率减小 |
| B、温度、压强均不变,充入HI气体,开始时正反应速率增大 |
| C、温度不变,压缩气体的体积,平衡不移动,颜色加深 |
| D、混和气体的密度不变,表示该反应达到平衡状态 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.1mol Fe与0.1mol Cl2充分反应,转移的电子数为0.3NA |
| B、1mol H2O2完全分解生成H2O和O2时,转移了NA个电子 |
| C、1mol C10H22分子中,含有共价键数目为32NA |
| D、0.5mol Na2O2中含有NA个阴离子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
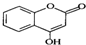 是一种医药中间体,常用来制备抗凝血药,可通过下列路线合成
是一种医药中间体,常用来制备抗凝血药,可通过下列路线合成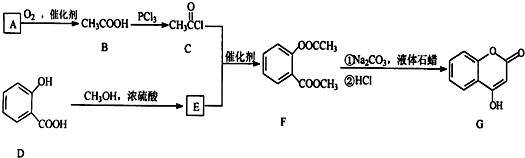
查看答案和解析>>
科目:高中化学 来源: 题型:
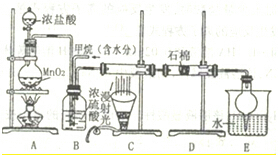
| V(Cl2) |
| V(CH4) |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
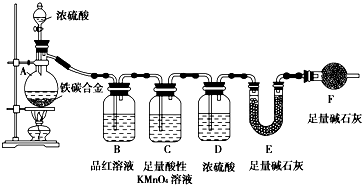 现有铁、碳两种元素组成的合金,某实验小组为了研究该合金的性质并测定该合金中碳的质量分数,设计了如下实验方案和实验装置:
现有铁、碳两种元素组成的合金,某实验小组为了研究该合金的性质并测定该合金中碳的质量分数,设计了如下实验方案和实验装置:| 滴加的溶液 | 氯水 | 氨水 |
| 沉淀的化学式 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com