
| A. | 64种 | B. | 8种 | C. | 32种 | D. | 16种 |
分析 X的分子式为C5H12O,能与金属钠反应产生氢气,说明X为戊醇,书写戊基-C5H11异构体,戊基异构数目等于戊醇的异构体数目;C5H12O的分子量为88,和它相对分子质量相同的一元羧酸为丁酸;生成酯的种类为醇和羧酸种类的乘积.
解答 解:X的分子式为C5H12O,能与金属钠反应产生氢气,说明X为戊醇,戊基-C5H11可能的结构有:-CH2CH2CH2CH2CH3、-CH(CH3)CH2CH2CH3、-CH(CH2CH3)2、-CHCH(CH3)CH2CH3、-C(CH3)2CH2CH3、-C(CH3)CH(CH3)2、-CH2CH2CH(CH3)2、-CH2C(CH3)3,所以该有机物的可能结构有8种;
C5H12O的分子量为88,和它相对分子质量相同的一元羧酸为丁酸,丙基有2种结构,则丁酸有2种结构,所以生成的酯的种类有:8×2=16,故选D.
点评 本题考查了同分异构体数目的计算,题目难度中等,正确计算醇和羧酸的同分异构体数目为解答关键,注意掌握同分异构体的概念及书写原则.


科目:高中化学 来源: 题型:选择题
| A. | 原子核内有8个中子的氧离子:${\;}_{8}^{18}$O | |
| B. | 硫离子的结构示意图: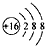 | |
| C. | NH4Cl的电子式: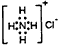 | |
| D. | 二氧化碳的结构式:O-C-O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
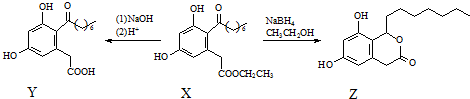
| A. | X、Y和Z中均不含手性碳原子 | |
| B. | Y能发生氧化、还原、取代、消去反应 | |
| C. | 一定条件下,1 mol X最多能与5 mol H2发生加成反应 | |
| D. | 1 mol Z最多可与含3 mol NaOH的溶液反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
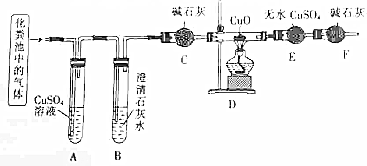
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 13种 | B. | 10种 | C. | 12种 | D. | 8种 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com