
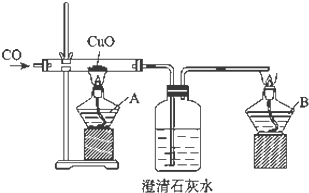
 证明CO具有还原性的实验装置,如图所示.
证明CO具有还原性的实验装置,如图所示.
| ||
| ||


科目:高中化学 来源: 题型:
| A、一种纯净的化合物 |
| B、一种单质和一种化合物的混合物 |
| C、两种化合物的混合物 |
| D、两种单质的混合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、3:2:2 |
| B、1:3:3 |
| C、2:3:6 |
| D、3:1:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
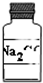 固体A的试剂瓶签已部分被腐蚀(如图所示).已知固体A只可能是Na2CO3、Na2SO3和Na2SO4中的一种.若取少量固体A配成稀溶液进行实验鉴定,下列说法错误的是( )
固体A的试剂瓶签已部分被腐蚀(如图所示).已知固体A只可能是Na2CO3、Na2SO3和Na2SO4中的一种.若取少量固体A配成稀溶液进行实验鉴定,下列说法错误的是( )| A、只用盐酸一种试剂就可以确定该固体A的成分 |
| B、依次加入Ba(NO3)2溶液、盐酸,若有白色沉淀,则固体A为Na2SO4 |
| C、滴入酸性KMnO4溶液,若KMnO4溶液褪色,则固体A为Na2SO3 |
| D、用pH试纸检验(常温),若pH>7,则固体A可能是Na2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、一定无Na2CO3,可能有FeCl3 |
| B、可能有Na2CO3和NaCl |
| C、一定有MgCl2,可能有NaCl |
| D、一定有NaCl |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
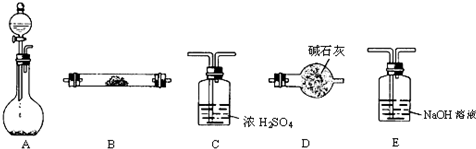
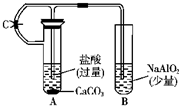 利用如图所示装置进行相关试验,验证铝的化合物的相关性质.请回答:
利用如图所示装置进行相关试验,验证铝的化合物的相关性质.请回答:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com