
| A. | 6种 | B. | 8种 | C. | 10种 | D. | 12种 |
分析 先根据异戊烷的结构写出一氯代物的种类,然后根据一氯代物中的种类来确定二氯代物的种类.
解答 解:异戊烷的一氯代物有4种:(CH3)2CHCH2CH2Cl、(CH3)2CHCHClCH3、(CH3)2CClCH2CH3、CH2Cl(CH3)CHCH2CH3;
当一氯代物为(CH3)2CHCH2CH2Cl时,二氯代物有4种:(CH3)2CHCH2CHCl2、(CH3)2CHCHClCH2Cl、(CH3)2CClCH2CH2Cl、CH2Cl(CH3)CHCH2CH2Cl;
当一氯代物为(CH3)2CHCHClCH3时,二氯代物有3种:(CH3)2CHCCl2CH3、(CH3)2CClCHClCH3、CH2ClCH(CH3)CHClCH3;
当一氯代物为(CH3)2CClCH2CH3时,二氯代物有1种:CH2ClC(CH3)ClCH2CH3;
当一氯代物为CH2Cl(CH3)CHCH2CH3时,二氯代物有2种:CHCl2CH(CH3)CH2CH3、(CH2Cl)2CHCH2CH3;
所以异戊烷的二氯代物的同分异构体共有10种;
故选C.
点评 本题难度较大,侧重对学生能力的培养,做题注意先判断该有机物中有几个等效氢原子,先固定一个氯原子的位置(生成一个一氯代物),然后对其二氯代物可能的情况进行书写.


科目:高中化学 来源: 题型:选择题
| A. | 在粗盐提纯中,当加热到蒸发皿中有较多固体析出,残留少量液体时,停止加热,用余热将液体蒸干 | |
| B. | 当振荡分液漏斗中的混合溶液时,须用一只手压住分液漏斗的玻璃塞,另一只手握住旋塞,将分液漏斗倒转过来,用力振荡 | |
| C. | 从加碘盐中获取碘单质的操作步骤为:溶解-萃取-分液-蒸馏 | |
| D. | 实验过程中若皮肤不慎沾上少量碱液,应先用大量水冲洗,再用2%醋酸溶液或饱和硼酸溶液洗,最后用水冲洗 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 周期表中有A、B、C三种原子序数依次增大的元素,A是地壳中含量最多的金属元素,B的价层电子排布为nsn-1npn+1,C是生活中的一种常用金属且其原子的外围电子排布为3d104s1.
周期表中有A、B、C三种原子序数依次增大的元素,A是地壳中含量最多的金属元素,B的价层电子排布为nsn-1npn+1,C是生活中的一种常用金属且其原子的外围电子排布为3d104s1.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 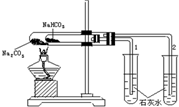 用如图装置比较Na2CO3与NaHCO3的稳定性 | |
| B. |  用如图装置吸收NH3,并防止倒吸 | |
| C. | 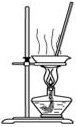 用如图装置蒸干AlCl3饱和溶液制备AlCl3晶体 | |
| D. | 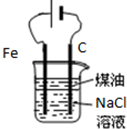 用如图装置制取Fe(OH)2沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 图I表示盐酸滴加到0.1mol/L某碱溶液中得到的滴定曲线,由图I可知二者恰好中和时,所得溶液的pH=7 | |
| B. | 图II表示一定条件下进行的反应2SO2+O2?2SO3△H<0各成分的物质的量变化,t2时刻改变的条件可能是加压或降低温度 | |
| C. | 图III表示某明矾溶液中加入Ba(OH)2溶液,沉淀的质量与加入Ba(OH)2溶液体积的关系,在加入20ml Ba(OH)2溶液时,沉淀是Al(OH)3与BaSO4的混合物 | |
| D. | 图IV表示向一定体积含等浓度NH4Cl、AlCl3、MgCl2混合溶液中逐渐加入NaOH溶液至过量的过程中,生成沉淀的质量与加入NaOH溶液的体积之间的关系 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
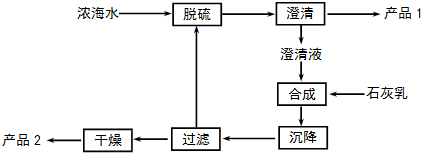
| 离子 | Na+ | Mg2+ | Cl- | SO42- |
| 浓度/(g•L-1) | 63.7 | 28.8 | 144.6 | 46.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

| TiCl4 | Mg | MgCl2 | Ti | |
| 熔点/℃ | -25.0 | 648.8 | 714 | 1667 |
| 沸点/℃ | 136.4 | 1090 | 1412 | 3287 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铝需经过特别处理能具有抗腐蚀能力 | |
| B. | “地沟油”经过加工处理可用来制肥皂 | |
| C. | 嫦娥系列卫星中使用的碳纤维,是一种新型无机非金属材料 | |
| D. | 只要符合限量,“食用色素”、“亚硝酸盐”可以作为某些食品的添加剂 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com