
| ① | ② | ③ | ④ | |
| pH | 11 | 11 | 3 | 3 |
| 溶液 | 氨水 | 氢氧化钠溶液 | 醋酸 | 盐酸 |
| A、①、④两溶液等体积混合,所得溶液中c(Cl-)>c(NH4+)>c(OH-)>c(H+) |
| B、分别加水稀释10倍,四种溶液的pH ①>②>④>③ |
| C、①、②中分别加入适量的氯化铵晶体后,两溶液的pH均减小 |
| D、VaL④与VbL②溶液混合后,若混合后溶液pH=4,则Va:Vb=11:9 |
| Va×0.001mol/L-Vb×0.001mol/L |
| Va+Vb |


科目:高中化学 来源: 题型:
| A、②⑤ | B、④⑤ |
| C、①③⑤ | D、③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
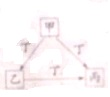
| A、若丁为KOH溶液,则甲可能为Al |
| B、若丁为Fe,则丙可能为Fe(NO3)2溶液 |
| C、若丁为O2,则甲可为非金属单质硫 |
| D、若甲、乙、丙均为焰色反应呈黄色的化合物,则丁一定为CO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CO2和Na2O2反应生成Na2CO3,推测:SO2和Na2O2反应生成Na2SO3 |
| B、金属钠着火不能用CO2扑灭,推测:金属钾着火也不能用CO2扑灭 |
| C、Fe3O4可表示为FeO?Fe2O3,推测:Pb3O4也可表示为PbO?Pb2O3 |
| D、F、Cl、Br,、I的单质熔点依次升高,推测N、P、As、Sb、Bi单质熔点也依次升高 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、混合物中铁单质物质的量的范围:0.03 mol<n(Fe)<0.07 mol |
| B、往得到的溶液中加入NaOH溶液现象为白色沉淀转化为灰绿色最后变为红褐色 |
| C、混合物里FeO的量无法确定,也不好比较Fe物质的量和Fe2O3物质的量的多少 |
| D、反应后所得溶液中的Fe2+与Cl-的物质的量之比为1:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
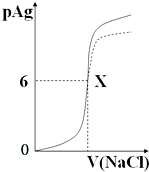 已知:pAg=-lg{c(Ag+)},KspAgCl=1×10-12如图是向10mLAgNO3溶液中逐渐加入0.1mol/L的NaCl溶液时,溶液的pAg随着加入NaCl溶液的体积(单位mL)变化的图象(实线).根据图象所得下列结论正确的是( )(提示:KspAgCl>KspAgI)
已知:pAg=-lg{c(Ag+)},KspAgCl=1×10-12如图是向10mLAgNO3溶液中逐渐加入0.1mol/L的NaCl溶液时,溶液的pAg随着加入NaCl溶液的体积(单位mL)变化的图象(实线).根据图象所得下列结论正确的是( )(提示:KspAgCl>KspAgI)| A、原AgNO3溶液的物质的量浓度为0.1 mol?L-1 |
| B、图中x点的坐标为(10,6 ) |
| C、图中x点表示溶液中Ag+ 与Cl-浓度相同 |
| D、把0.1 mol?L-1的NaCl换成0.1 mol?L-1NaI则图象在终点后变为虚线部分 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、称氢氧化钠时,不能直接称量,要放在称量纸上 |
| B、蒸馏时,应使温度计水银球靠近蒸馏烧瓶的支管口处 |
| C、分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 |
| D、过滤时,玻璃棒的末端应轻轻靠在三层的滤纸上 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com