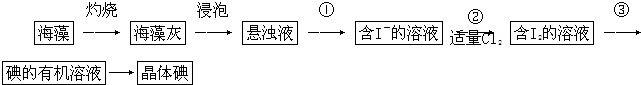
“低碳循环”已引起各国家的高度重视,而如何降低大气中CO
2的含量和有效地开发利用CO
2正成为化学家研究的主要课题.
(1)用电弧法合成的储氢纳米碳管常伴有大量的碳纳米颗粒(杂质),这种颗粒可用如下氧化法提纯,请完成该反应的化学方程式:
C+
KMnO
4+
H
2SO
4→
CO
2↑+
MnSO
4+
K
2SO
4+
H
2O
(2)将不同量的CO(g)和H
2O(g)分别通入到体积为2L的恒容密闭容器中,进行反应CO(g)+H
2O(g)?CO
2(g)+H
2(g),得到如下三组数据:
| 实验组 | 温度℃ | 起始量/mol | 平衡量/mol | 达到平衡所需要时间/min |
| CO | H2O | H2 | CO |
| 1 | 650 | 4 | 2 | 1.6 | 2.4 | 6 |
| 2 | 900 | 2 | 1 | 0.4 | 1.6 | 3 |
| 3 | 900 | a | b | c | d | t |
①实验2条件下平衡常数K=
.
②实验3中,若平衡时,CO的转化率大于水蒸气,则a/b的值
(填具体值或取值范围).
③实验4,若900℃时,在此容器中加入CO、H
2O、CO
2、H
2均为1mol,则此时V正
V逆(选填“<”,“>”或“=”).
(3)已知在常温常压下:
①2CH
3OH(l)+3O
2(g)=2CO
2(g)+4H
2O(g)△H=-1275.6kJ?mol-1
②2CO(g)+O
2(g)=2CO
2(g)△H=-566.0kJ?mol-1
③H
2O(g)=H
2O(l)△H=-44.0kJ?mol-1
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:
.
(4)CO
2在自然界循环时可与CaCO
3反应,CaCO
3是一种难溶物质,其Ksp=2.8×10-9.CaCl2溶液与Na
2CO3溶液混合可形成CaCO
3沉淀,现将等体积的CaCl
2溶液与Na
2CO
3溶液混合,若Na
2CO
3溶液的浓度为1×10
-4 mo1/L,则生成沉淀所需CaCl
2溶液的最小浓度为
mo1/L.
(5)最近科学家再次提出“绿色化学”构想:把空气吹入碳酸钾溶液,然后再把CO
2从溶液中提取出,经化学反应后使空气中的CO
2转变为可再生燃料甲醇.甲醇可制作燃料电池,写出以稀硫酸为电解质甲醇燃料电池负极反应式
.当电子转移的物质的量为0.6mol时,参加反应的氧气的体积是
L(标准状况下).



 全优冲刺100分系列答案
全优冲刺100分系列答案 英才点津系列答案
英才点津系列答案 红果子三级测试卷系列答案
红果子三级测试卷系列答案 某实验小组欲制取乙酸乙酯,设计了如下图所示的装置,请回答有关问题:
某实验小组欲制取乙酸乙酯,设计了如下图所示的装置,请回答有关问题: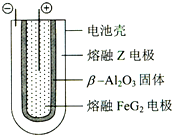 有X、Y、Z、M、G五种元素,是分属三个短周期并且原子序数依次增大的主族元素.其中X、Z同主族,可形成离子化合物ZX;Y、M同主族,可形成MY2、MY3两种分子.完成下列填空:
有X、Y、Z、M、G五种元素,是分属三个短周期并且原子序数依次增大的主族元素.其中X、Z同主族,可形成离子化合物ZX;Y、M同主族,可形成MY2、MY3两种分子.完成下列填空: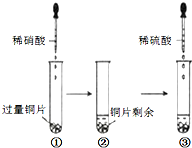 某实验过程如图所示,则图③试管中的现象是( )
某实验过程如图所示,则图③试管中的现象是( )