
| n |
| V |


 步步高达标卷系列答案
步步高达标卷系列答案科目:高中化学 来源: 题型:
| A、常温下,pH=7的NH4Cl与氨水的混合溶液:c(H+)=c(OH-)=c(NH4+)=c(Cl-) |
| B、0.1mol/LNa2S溶液:c(OH-)=c(H+)+c(HS-)+c(H2S) |
| C、pH=a的氨水溶液,稀释10倍后,其pH=b,则a=b+1 |
| D、常温下,pH=2的CH3COOH与pH=12的NaOH等体积混合:c (CH3COO-)+c(H+)>c(Na+)+c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:

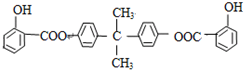
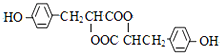
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、n(H2SO4)=0.6mol c(H2SO4)>6mol/L |
| B、n(H2SO4)=0.3mol c(H2SO4)≥3mol/L |
| C、n(H2SO4)<0.3mol c(H2SO4)<3mol/L |
| D、0.3mol≤n(H2SO4)≤0.6mol 3mol/L≤c(H2SO4)≤6mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、原子序数:W>Z>X>Y |
| B、离子半径:r(W2+)>r(X-)>r(Y2-)>r(Z+) |
| C、Y的气态氢化物比X的气态氢化物稳定 |
| D、氢氧化物碱性强弱:W(OH)2>ZOH |
查看答案和解析>>
科目:高中化学 来源: 题型:
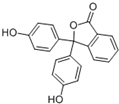
| A、分子式为C20H14O4 |
| B、可以发生取代反应、加成反应、氧化反应 |
| C、含有的官能团有羟基、酯基 |
| D、1mol该物质可与H2和溴水发生反应,消耗H2和Br2的最大值为10mol和4mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
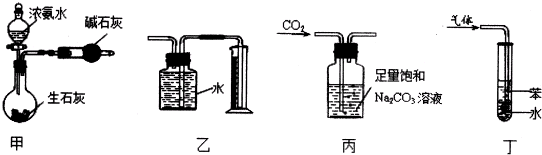
| A、甲装置制干燥的氨气 |
| B、用乙装置收集并测量Cu与浓硝酸反应产生的气体及体积 |
| C、用丙装置除去CO2中含有的少量HC1 |
| D、用丁装置吸收NH3,并防止倒吸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①③ | B、②④ | C、①④ | D、②③ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com