
在一定温度下的定容容器中,当下列哪些物理量不再发生变化时,表明反应A(g)+2B(g)  C(g)+D(g)已达到平衡状态
C(g)+D(g)已达到平衡状态
①混合气体的压强
②混合气体的密度
③B的物质的量浓度
④混合气体总物质的量
⑤混合气体的平均相对分子质量
⑥v(C)与v(D)的比值
⑦混合气体总质量
⑧混合气体总体积
A.①②③④⑤⑥⑦⑧ B.①⑤⑧
C.②⑤⑦ D.①③④⑤
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2016-2017学年广西省高二上9月月考化学卷(解析版) 题型:选择题
常温时,下列溶液的pH或微粒的物质的量浓度关系正确的是( )
A.某溶液中由水电离出的c(H+)=1×10-amol/L,若a>7 时,该溶液pH一定为14-a
B.0.1mol的KHA溶液,其pH=10, c(K+)>c(A2-)>c(HA-)>c(OH-)
C.将0.2mol/L的某一元酸HA溶液和0.1mol/LNaOH溶液等体积混合后溶液pH 大于7,则反应后的混合液:c(HA)> c(Na+)>c(A)
D.等体积、等物质的量浓度的Na2CO3溶液与NaHCO3溶液混合:3c(Na+)=2c(CO32-)+2c(HCO3-)+2c(H2CO3)
查看答案和解析>>
科目:高中化学 来源:2017届四川省高三上学期10月月考化学试卷(解析版) 题型:选择题
X、Y、Z、W是短周期主族元素,X原子最外层电子数是次外层的两倍,Y元素在地壳中的含量最多,Z元素的金属性最强,W原子的核外电子数是X原子与Z原子的核外电子数之和。下列叙述正确的是
A. X、Y、Z形成的化合物不止一种
B. X的氢化物比Y的氢化物稳定
C. 原子半径的大小顺序:r(W)>r(Z)>r(Y)>r(X)
D. Y与Z或W形成的化合物中只含离子键
查看答案和解析>>
科目:高中化学 来源:2017届四川省高三上学期10月阶段测化学卷(解析版) 题型:选择题
设 NA 表示阿伏加德罗常数的值,下列叙述正确的是
A.在反应 KClO3 + 6HCl = KCl + 3Cl2↑+ 3H2O 中,Cl2 既是氧化产物又是还原产物,当得到标准状况下的 67.2 L Cl2 时,反应中转移的电子数为 5NA
B.标准状况下,22.4 L 甲苯中含有的 C—H 键数目为 8NA
C.50 g 46%的乙醇水溶液中,含氢原子总数目为 3NA
D.t℃时,MgCO3 的 Ksp = 4×10-6,则该温度下饱和 MgCO3 溶液中含有的 Mg2+数目为 2×10-3NA
查看答案和解析>>
科目:高中化学 来源:2017届山西省高三上学期10月月考化学试卷(解析版) 题型:选择题
下列实验方案中,不能达到实验目的的是
选项 | 实验目的 | 实验方案 |
A | 除去CO2气体中的SO2气体 | 将混合气体通入饱和碳酸氢钠溶液,洗气 |
B | 检验Fe(NO3)2晶体是否已氧化变质 | 将Fe(NO3)2样品溶于稀H2SO4后,滴加KSCN溶液,观察溶液是否变红 |
C | 验证Br2的氧化性强于I2 | 强少量溴水加入KI溶液中,再加入CCl4,振荡,静置,可观察到下层液体呈紫色 |
D | 验证Fe(OH)3的溶解度小于Mg(OH)2 | 将FeCl3溶液加入Mg(OH)2悬浊液中,振荡,可观察到沉淀由白色变为红色 |
查看答案和解析>>
科目:高中化学 来源:2017届山西省高三上学期10月月考化学试卷(解析版) 题型:选择题
已知酸性条件下KMnO4可将乙醛氧化为乙酸,其反应的离子反应方程式如下:□MnO4- + □CH3CHO + □ = □Mn2+ + □CH3COOH + □ .如有1mol的氧化剂参与反应,则反应中转移的电子数目为
A.2mol B.10mol C.5mol D.7mol
查看答案和解析>>
科目:高中化学 来源:2017届湖南省长沙市高三上月考二化学试卷(解析版) 题型:实验题
硫酸亚锡(SnSO4)是一种重要的能溶于水的硫酸盐,广泛应用于镀锡工业。某研究小组设计SnSO4制备路线如下:
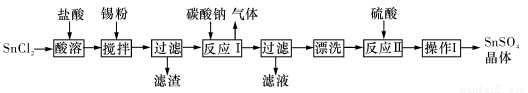
查阅资料:
I.酸性条件下,锡在水溶液中有Sn2+、Sn4+两种主要存在形式,Sn2+易被氧化。
Ⅱ.SnC12易水解生成碱式氯化亚锡[Sn(OH)Cl]
回答下列问题:
(1)操作I是____________。
(2)SnCl2粉末需加浓盐酸进行溶解,请结合必要的化学方程式用平衡移动原理解释原因:__________。
(3)加入Sn粉的作用有两个:①调节溶液pH;②__________。
(4)反应I得到沉淀SnO,得到该沉淀的离子反应方程式是____________。
(5)酸性条件下,SnSO4还可以用作双氧水去除剂,发生反应的离子方程式是:________________。
(6)该小组通过下列方法测定所用锡粉的纯度(杂质不参与反应):
①试样溶于盐酸中,发生的反应为:Sn+2HCl=SnCl2+H2;
②加入过量的FeC13;
③用已知浓度的K2Cr2O7滴定生成的Fe2+,发生的反应为:
6FeCl2+ K2Cr2O7+14HCl=6FeCl3+2KCl+2CrCl3+7H2O。
取1.226g锡粉,经上述各步反应后共用去0.100mol/L K2Cr2O7溶液32.0mL。锡粉中锡的质量分数是________。(保留三位有效数字)
查看答案和解析>>
科目:高中化学 来源:2017届湖南省长沙市高三上月考二化学试卷(解析版) 题型:选择题
把VL含有MgSO4和K2SO4的混合溶液分成两等份,一份加入含amolNaOH的溶液,恰好使镁离子完全沉淀为氢氧化镁;另一份加入含bmolBaCl2的溶液,恰好使硫酸根离子完全沉淀为硫酸钡。则原混合溶液中钾离子的浓度为
A.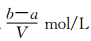 B.
B.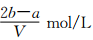 C.
C.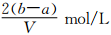 D.
D.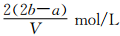
查看答案和解析>>
科目:高中化学 来源:2017届广西省高三上9月月考化学试卷(解析版) 题型:填空题
NaNO2外观和食盐相似,又有咸味,容易使人误食中毒。已知NaNO2能发生如下反应:
2NaNO2+4HI===2NO↑+I2+2NaI+2H2O。
(1)上述反应中氧化剂是________。
(2)根据上述反应,鉴别NaNO2和NaCl。可选用的物质有:①碘化钾淀粉试纸 ②淀粉 ③白酒④食醋,你认为应选用的物质有________(填序号)。
(3)某厂废液中,含有2%~5%的NaNO2,直接排放会造成污染,下列试剂能使NaNO2转化为不引起二次污染的N2的是________。
A.NaCl B.NH4Cl C.HNO3 D.浓H2SO4
(4)请配平以下化学方程式 Al+ NaNO3+ NaOH— N aAlO2+ N2↑+ H2O,若反应过程中转移5mol电子,则生成标准状况下N2的体积为________L。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com