
| A. | a<b | B. | a>b | C. | a=b | D. | 无法确定 |
分析 已知CuSO4•5H2O(s)=CuSO4(s)+5H2O(l);△H=+bKJ/mol;CuSO4(s)=Cu2+(aq)+SO42-(aq);△H=-akJ/mol;
胆矾溶于水时,溶液温度降低,反应为CuSO4•5H2O(s)=Cu2+(aq)+SO42-(aq)+5H2O(l)△H′>0;根据盖斯定律确定△H′与a、b的关系
解答 解:已知①CuSO4•5H2O(s)=CuSO4(s)+5H2O(l);△H=+bKJ/mol;
②CuSO4(s)=Cu2+(aq)+SO42-(aq);△H=-akJ/mol;
③CuSO4•5H2O(s)=Cu2+(aq)+SO42-(aq)+5H2O(l)△H′>0;
根据盖斯定律:方程③=方程①+方程②,
所以△H′=b+(-a)>0,即b>a,
故选A.
点评 本题考查了物质溶解恒容物质分解过程中的能量变化,根据盖斯定律分析物质溶解过程中的能量变化是解题关键,题目难度中等.


 小学课时作业全通练案系列答案
小学课时作业全通练案系列答案 金版课堂课时训练系列答案
金版课堂课时训练系列答案 单元全能练考卷系列答案
单元全能练考卷系列答案 新黄冈兵法密卷系列答案
新黄冈兵法密卷系列答案科目:高中化学 来源: 题型:解答题
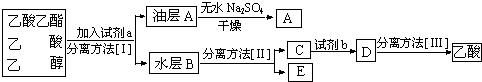
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 红、白、蓝 | B. | 黑、白、蓝 | C. | 白、白、蓝 | D. | 黑、红、蓝 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 鸡蛋清溶液滴入浓硝酸微热有黄色沉淀生成 | |
| B. | 采用多次盐析和溶解,可以分离提纯蛋白质 | |
| C. | 用稀释后的福尔马林浸泡种子会使蛋白质变性 | |
| D. | 蛋白质是仅由C、H、O三种元素组成的高分子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
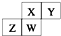 如图为元素周期表截取的短周期的一部分,四种元素均不是稀有气体元素.下列关于这四种元素及其化合物的说法中正确的是( )
如图为元素周期表截取的短周期的一部分,四种元素均不是稀有气体元素.下列关于这四种元素及其化合物的说法中正确的是( )| A. | 原子半径:W>Z>Y>X | |
| B. | 气态氢化物的稳定性:Z>W>X>Y | |
| C. | z的最高正化合价与最低负化合价的绝对值可能相等 | |
| D. | w的最高价氧化物的水化物可能为弱酸,也有可能为强酸 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com