
分析 (1)①将已知方程式变形:$\frac{①×2-②}{3}$得目标方程式:2H2S(g)+O2(g)=2H2O(g)+2S(s),依据盖斯定律计算反应热;
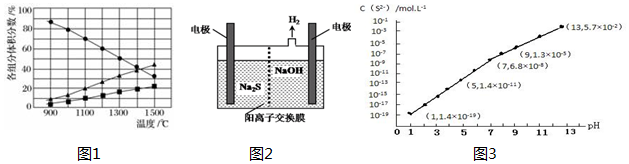
(2)①依据题干可知:H2S在高温下分解生成氢气、S,结合图中数据可知反应为可逆反应,依据原子个数、得失电子数守恒书写方程式;
②依据图表中达到平衡时各物质的百分含量,列三段计算反应平衡常数;
(3)①电解池阴极发生还原反应,图中阴极区为氢氧化钠溶液,则水电离产生的氢离子得到电子生成氢气,据此书写电极反应式;
②硫化钠为强碱弱酸盐,硫离子水解而使其溶液呈碱性,硫离子有两步水解,第一步水解能力远远大于第二步;
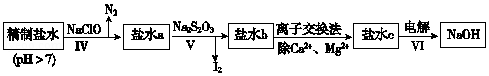
(4)①pH=13时,c(S2-)=5.7×10-2mol/L,在0.10mol•L-1H2S溶液中根据硫守恒c(H2S)+c(HS-)+c(S2-)=0.10mol•L-1;
②当Qc=Ksp(MnS)时开始沉淀,由此求出硫离子的浓度,结合图象得出此时的pH;
解答 解:(1)已知①脱硫:Fe2O3•H2O(s)+3H2S(g)=Fe2S3•H2O(s)+3H2O(g)△H=-akJ/mol
②再生:2Fe2S3•H2O(s)+3O2(g)=2Fe2O3•H2O(s)+6S(s)△H=-bkJ/mol
则得到2H2S(g)+O2(g)=2H2O(g)+2S(s),依据盖斯定律可知反应的焓变为:-$\frac{(2a+b)}{3}$ kJ/mol;
故答案为:-$\frac{(2a+b)}{3}$ kJ/mol;
(2)①依据题干可知:H2S在高温下分解生成氢气、S,结合图中数据可知反应为可逆反应依据原子个数、得失电子数守恒可知反应的方程式:2H2S(g)?2H2(g)+S2(g);
故答案为:2H2S(g)?2H2(g)+S2(g);
②据图1计算;若1400℃时,VL恒容容器中加入amol的H2S,达到平衡时,硫化氢、氢气体积分数为40%,S2(g)的体积分数为:20%,设生成的S2(g)物质的量为xmol,则:
2H2S(g)?2H2(g)+S2(g)
a 0 0
2x 2x x
a-2x 2x x
达到平衡时,硫化氢、氢气体积分数相等,即a-2x=2x,解得x=$\frac{a}{4}$;
则平衡时,H2S物质的量浓度为:$\frac{a}{2V}$mol/L,H2物质的量浓度为:$\frac{a}{2V}$mol/L,S2物质的量浓度为:$\frac{a}{4V}$mol/L,
则反应平衡常数为:$\frac{\frac{a}{4V}×\frac{a}{2V}×\frac{a}{2V}}{\frac{a}{2V}×\frac{a}{2V}}$=$\frac{a}{4V}$;
故答案为:$\frac{a}{4V}$;
(3)①电解池阴极发生还原反应,图中阴极区为氢氧化钠溶液,则水电离产生的氢离子得到电子生成氢气,电极反应式:2H2O+2e-=H2↑+2OH-;
故答案为:2H2O+2e-=H2↑+2OH-;
②硫化钠为强碱弱酸盐,硫离子易水解而使其溶液呈碱性,硫离子第一步水解能力远远大于第二步,溶液中氢氧根离子来源于水的电离和硫离子水解,硫氢根离子只来源于硫离子水解,但硫离子的水解能力较小,所以溶液中离子浓度大小顺序是c(Na+)>c(S2-)>c(OH-)>c(HS-)>C(H+);
故答案为:c(Na+)>c(S2-)>c(OH-)>c(HS-)>C(H+);
(4))①根据溶液pH与c(S2-)关系图pH=13时,c(S2-)=5.7×10-2mol/L,在0.10mol•L-1H2S溶液中根据硫守恒c(H2S)+c(HS-)+c(S2-)=0.10mol•L-1,所以c(H2S)+c(HS-)=0.1-5.7×10-2=0.043mol/L,
故答案为:0.043;
②当Qc=Ksp(MnS)时开始沉淀,所以c(S2-)=$\frac{Ksp(MnS)}{c(M{n}^{2}{\;}^{+})}$=$\frac{2.8×10{\;}^{-13}}{0.020}$mol/L=1.4×10-11mol/L,结合图象得出此时的pH=5,所以pH=5时锰离子开始沉淀,
故答案为:5.
点评 本题为综合题,考查了反应热的计算、方程式的书写、化学平衡常数的计算、离子浓度大小的比较、电极反应式的书写、pH值的计算,题目综合性强,难度较大,熟悉盖斯定律计算反应热的方法、化学平衡常数的计算、电解池原理、盐类水解的规律是解题关键.


 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案科目:高中化学 来源: 题型:多选题
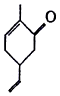
| A. | 可以发生氧化反应 | B. | 分子式为C9H10O | ||
| C. | 分子中所有原子都处于同一平面上 | D. | 能使溴的四氯化碳溶液褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| X | Y | |
| Z |
| A. | Y的单质与水反应时,Y的单质既是氧化剂又是还原剂 | |
| B. | X的最高价氧化物对应的水化物与其气态氢化物可以反应生成盐 | |
| C. | X、Y、Z元素形成的单质,常温下Z单质的沸点最底 | |
| D. | X的氢化物只有一种 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| CaSO4 | Mg2(OH)2CO3 | CaCO3 | BaSO4 | BaCO3 |
| 2.6×10-2 | 2.5×10-4 | 7.8×10-4 | 2.4×10-4 | 1.7×10-3 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 .该反应中还原剂是KI,21.4g KIO3参加反应时转移电子0.5mol.
.该反应中还原剂是KI,21.4g KIO3参加反应时转移电子0.5mol.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 同分异构现象只存在于有机物和无机物之间 | |
| B. | 同分异构现象不存在于无机物之间 | |
| C. | 在无机化合物和有机化合物间一定存在同分异构现象 | |
| D. | 在无机化合物和有机化合物间可能存在同分异构现象 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下,5.6g金属铁投入足量的浓硫酸中,电子转移数为0.3NA | |
| B. | 18g D2O所含的中子数为10NA | |
| C. | 标准状况下,8 gSO3所含原子数为0.4NA | |
| D. | 常温下,1.0LpH=13的Ba (OH) 2溶液中含有的OH-数目为0.2NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com