
| 编号 | 电极材料 | 电解质溶液 | 电流计指针偏转方向 |
| ① | Mg Al | 稀盐酸 | 偏向Al |
| ② | Al Cu | 稀盐酸 | 偏向Cu |
| ③ | Al 石墨 | 稀盐酸 | 偏向石墨 |
| ④ | Mg Al | NaOH溶液 | 偏向Mg |
| ⑤ | Al Cu | 浓硝酸 | 偏向Al |
分析 (1)金属与酸构成的原电池中,活泼金属作负极,据此对实验①、②进行判断;
(2)实验③中Al为负极,石墨为正极,电池反应为2Al+6HCl═2AlCl3+3H2↑;
(3)根据实验①、②2可知,原电池的正负极取决于金属的活泼性强弱;根据实验④可知,原电池的正负极与电解质溶液的酸碱性有关;
(4)实验5中Al遇浓硝酸发生钝化,发生Cu与浓硝酸的氧化还原反应,Cu作负极,Al作正极,所以电流计指针偏向铝.
解答 解:(1)金属与酸构成的原电池中,活泼金属作负极,则实验①中Mg的活泼性大于Al,所以Al作正极,而实验②中Al的活泼性大于Cu,所以Al作负极,所以实验①、②的Al所作的电极分别是:正极、负极,故d正确,
故答案为:d;
(2)实验③中Al为负极,电极反应为:2Al-6e-═2Al3+,
石墨为正极,其电极反应为:6H++6e-═3H2↑,
电池总反应为:2Al+6HCl═2AlCl3+3H2↑,
故答案为:2Al-6e-═2Al3+; 6H++6e-═3H2↑;
(3)根据表中实验结果可知,在原电池中电极作正极还是负极,与两个电极的相等活泼性有关,也与电解质溶液的酸碱性有关,
故答案为:两个电极的相对活泼性;电解质溶液的酸碱性;
(4)实验⑤中Al遇浓硝酸发生钝化,发生Cu与浓硝酸的氧化还原反应,Cu作负极,Al作正极,电流由正极流向负极,所以电流计指针偏向铝,
故答案为:常温下在浓硝酸中,Al钝化作正极,铜易失电子作负极,所以电流计指针偏向铝.
点评 本题考查原电池原理、电极反应方程式的书写,题目难度中等,明确发生的原电池反应及正负极的判断是解答本题的关键,注意掌握利用氧化还原反应中化合价变化判断原电池的正负极的方法.


科目:高中化学 来源: 题型:填空题

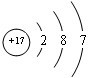 .
.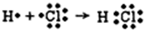 .
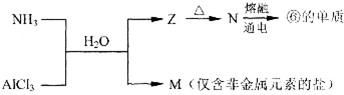
.
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 (Ⅰ)用纯净的碳酸钙与稀盐酸反应制取二氧化碳气体,请回答:
(Ⅰ)用纯净的碳酸钙与稀盐酸反应制取二氧化碳气体,请回答:| 时间(s) 物质的量浓度(mol/L) 物质 | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 |
| SO2 | 1 | 0.7 | 0.5 | 0.35 | 0.2 | 0.1 | 0.1 | 0.1 |
| O2 | 0.5 | 0.35 | 0.25 | 0.18 | 0.1 | 0.05 | 0.05 | 0.05 |
| SO3 | 0 | 0.3 | 0.5 | 0.65 | 0.8 | 0.9 | 0.9 | 0.9 |
| 压强 转化率 温度 | 0.1MPa | 0.5MPa | 1MPa | 10MPa |
| 400℃ | 99.2 | 99.6 | 99.7 | 99.9 |
| 500℃ | 93.5 | 96.9 | 97.8 | 99.3 |
| 600℃ | 73.7 | 85.8 | 90.0 | 96.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,11.2 L的戊烷所含的分子0.5NA | |
| B. | 28 g乙烯所含共用电子对数目为4NA | |
| C. | 标准状况下,11.2 L二氯甲烷所含分子数为0.5 NA | |
| D. | 现有乙烯、丙烯、丁烯的混合气体共14 g,其原子数为3 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验步骤 | 实验操作 | 预期现象及结论 |
| 1 | 取少量所得溶液于试管中, 再滴入几滴稀盐酸 | 若无气泡产生,证明原溶液中不含有Na2CO3 |
| 2 | 另取少量所得溶液于试管中, 再滴入几滴Na2CO3溶液 | 若无沉淀产生,结合步骤1,猜想一成立. |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 NH4+
NH4+
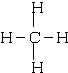 ; CO2O=C=O
; CO2O=C=O I.
I.
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 小苏打可以治疗胃酸过多,是利用了小苏打的酸性 | |
| B. | 与足量等浓度盐酸溶液反应的速率:NaHCO3<Na2CO3 | |
| C. | 久置在空气中的钠最后变成碳酸钠晶体 | |
| D. | 某未知样品灼烧时能使火焰呈黄色,说明该样品中肯定含有钠元素 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com