
| A. | 醋酸溶液能使紫色石蕊溶液变红 | |
| B. | 醋酸溶液能与碳酸钠反应产生二氧化碳气体 | |
| C. | 煮沸醋酸溶液再冷却到常温,发现溶液pH变大 | |
| D. | 浓度均为1mol/L的盐酸和醋酸,前者导电能力强 |
分析 要证明醋酸为弱酸,可证明存在电离平衡、不能完全电离或从对应的强碱盐溶液呈碱性的角度,以此解答该题.
解答 解:A.强酸、弱酸溶液都能使紫色石蕊溶液变红,不能判断醋酸为弱电解质,故A错误;
B.强酸和弱酸溶液都能与碳酸钠反应产生二氧化碳气体,不能说明醋酸为弱电解质,故B错误;
C.煮沸醋酸溶液再冷却到常温,醋酸挥发,溶液中氢离子难度减小溶液pH变大,不能说明醋酸为弱电解质,故C错误;
D.相同浓度的一元酸醋酸和盐酸溶液醋酸导电性弱,说明醋酸溶液存在电离平衡为弱电解质,故D正确;
故选D.
点评 本题考查了弱电解质的判断,题目难度不大,电解质强弱是根据其电离程度划分的,不能根据溶液导电性强弱划分,为易错点.


科目:高中化学 来源: 题型:选择题
| A. | 加入水时,溶液中离子浓度都减小 | |
| B. | 加入少量NaOH固体,平衡向正反应方向移动 | |
| C. | 加入少量0.1mol•L-1CH3COOH溶液,溶液中c(H+)减小 | |
| D. | 加入少量CH3COONa固体,电离平衡常数减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
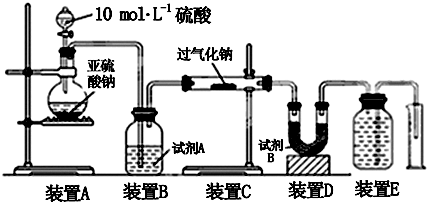
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 同种元素的原子均有相同的质子数和中子数 | |
| B. | 微粒Na+、Mg2+、O2-具有相同的电子层结构 | |
| C. | 短周期第ⅣA与ⅥIA族元素的原子间构成的分子,均满足原子最外层8电子结构 | |
| D. | ${\;}_{20}^{48}$Ca2+的中子数比核外电子数多10 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下,Ag2SO4、AgCl、AgI在水中溶解能力依次减弱 | |
| B. | 在AgCl饱和溶液中加入NaI固体,有AgI沉淀生成 | |
| C. | 在AgCl饱和溶液中加入NaI固体,有AgI沉淀生成 | |
| D. | 因为AgCl比Ag2SO4更难溶,所以AgCl不会转化为Ag2SO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 该有机物的分子式为C11H14O3 | |
| B. | 该有机物可能易溶于水且具有水果香味 | |
| C. | 该有机物可能发生的化学反应类型有:水解、酯化、氧化、取代 | |
| D. | 1mol该有机物在Ni作催化剂的条件下能与4molH2发生加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
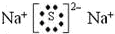
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 海水$\stackrel{NaOH}{→}$Mg(OH)2$\stackrel{电解}{→}$Mg | |
| B. | 海水$\stackrel{HCl}{→}$MgCl2溶液→MgCl2晶体$\stackrel{电解}{→}$Mg | |
| C. | 海水$\stackrel{石灰乳}{→}$Mg(OH)2$\stackrel{灼烧}{→}$MgO$\stackrel{电解}{→}$Mg | |
| D. | 海水$\stackrel{石灰乳}{→}$Mg(OH)2$\stackrel{HCl}{→}$MgCl2溶液-→MgCl2晶体(熔融)$\stackrel{电解}{→}$Mg |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com