
| A£® | ÖĮÉŁ“ęŌŚ5ÖÖĄė×Ó | |
| B£® | SO42”„”¢NH4+Ņ»¶Ø“ęŌŚ£¬Cl”„æÉÄܲ»“ęŌŚ | |
| C£® | Cl”„Ņ»¶Ø“ęŌŚ£¬ĒŅc£ØCl”„£©”Ż0.3mol/L | |
| D£® | CO32”„”¢Al3+Ņ»¶Ø²»“ęŌŚ£¬K+æÉÄÜ“ęŌŚ |
·ÖĪö ¼ÓČė¹żĮæNaOHČÜŅŗ£¬¼ÓČČ£¬µĆµ½448mLĘųĢ壬ĪļÖŹµÄĮæĪŖ0.02mol£¬æÉÖŖŅ»¶Ø“ęŌŚļ§øłĄė×Ó£¬ŗģŗÖÉ«³ĮµķŹĒĒāŃõ»ÆĢś£¬3.2g¹ĢĢåĪŖČżŃõ»Æ¶žĢś£¬æÉÖŖŅ»¶ØÓŠFe3+£¬Ņ»¶ØƻӊCO32-£»
9.32g²»ČÜÓŚŃĪĖįµÄ³Įµķ£¬ĪŖĮņĖį±µ³Įµķ£¬ĪļÖŹµÄĮæĪŖ£ŗ0.04mol£¬øł¾ŻŅŌÉĻŹż¾ŻĶĘĖć“ęŌŚĄė×Ó£¬øł¾ŻµēŗÉŹŲŗćĶĘĖćĀČĄė×ӵēęŌŚ¼°Źż¾Ż£®
½ā“š ½ā£ŗ¼ÓČė¹żĮæNaOHČÜŅŗ£¬¼ÓČČ£¬µĆµ½448mLĘųĢ壬ĪļÖŹµÄĮæĪŖ$\frac{0.448L}{22.4L/mol}$=0.02mol£¬æÉÖŖŅ»¶Ø“ęŌŚļ§øłĄė×Ó£¬ŗģŗÖÉ«³ĮµķŹĒĒāŃõ»ÆĢś£¬3.2g¹ĢĢåĪŖČżŃõ»Æ¶žĢś£¬æÉÖŖŅ»¶ØÓŠFe3+£¬Ņ»¶ØƻӊCO32-£¬ĒŅn£ØFe2O3£©=$\frac{3.2g}{160g/mol}$=0.02mol£¬æÉÖŖn£ØFe3+£©=0.04mol£¬
9.32g²»ČÜÓŚŃĪĖįµÄ³Įµķ£¬ĪŖĮņĖį±µ³Įµķ£¬ĪļÖŹµÄĮæĪŖ£ŗ$\frac{9.32g}{233g/mol}$=0.04mol£¬
A£®A£®ÓÉÉĻŹö·ÖĪöæÉÖŖ£¬Ņ»¶Øŗ¬SO42-”¢NH4+”¢Fe3+£¬ČÜŅŗÖŠNH4+”¢Fe3+Ėł“ųÕżµēŗÉĪŖ0.02mol+3”Į0.04mol=0.14mol£¬SO42-Ėł“ųøŗµēŗÉĪŖ2”Į0.04mol=0.08mol£¬¾ŻµēŗÉŹŲŗć£¬ÖŖČÜŅŗÖŠ±ŲČ»“óĮæ“ęŌŚĮķŅ»ÖÖŅõĄė×ÓCl-£¬ŌņÖĮÉŁ“ęŌŚ4ÖÖĄė×Ó£¬¹ŹA“ķĪó£»
B£®ÓÉÉĻŹö·ÖĪöæÉÖŖ£¬SO42-”¢NH4+Ņ»¶Ø“ęŌŚ£¬ĒŅÓÉAæÉÖŖŗ¬ÓŠCl-£¬¹ŹB“ķĪó£»
C£®ÓɵēŗÉŹŲŗćæÉÖŖ£¬Cl-Ņ»¶Ø“ęŌŚ£¬ĒŅc£ØCl-£©”Ż0.14mol-0.08mol=0.06mol£¬ÅØ¶Č“óÓŚ0.3mol/L£¬¹ŹCÕżČ·£»
D£®×ŪÉĻĖłŹö£¬ŌČÜŅŗÖŠŅ»¶Øŗ¬Fe3+”¢NH4+”¢SO42-ŗĶCl-£¬æÉÄÜŗ¬Al3+”¢K+£¬Ņ»¶Ø²»ŗ¬CO32-£¬¹ŹD“ķĪó£®
¹ŹŃ”C£®
µćĘĄ ±¾Ģāæ¼²éĪļÖŹµÄ¼ģŃé¼°ĶʶĻ£¬ĪŖøßæ¼³£¼ūĢāŠĶŗĶøßĘµæ¼µć£¬²ąÖŲÓŚŌŖĖŲ»ÆŗĻĪļÖŖŹ¶µÄ×ŪŗĻĄķ½āŗĶŌĖÓƵÄ漲飬עŅā³£¼ūĄė×ӵĊŌÖŹŗĶ·“Ó¦ĄąŠĶµÄÅŠ¶Ļ£¬“šĢāŹ±ČĻÕęŌĶĮ”¢·ÖĪöĢāÖŠŹż¾Ż£¬ŗĻĄķ·ÖĪö£¬ĢŲ±šŹĒĀČĄė×ÓµÄĶʶĻ£¬ĢāÄæÄѶČÖŠµČ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĪŽ·ØÅŠ¶Ļ¹ĢĢåÖŠFeCl2ŹĒ·ń“ęŌŚ | |
| B£® | ¢ŪÖŠŹ¹øßĆĢĖį¼ŲČÜŅŗĶŹÉ«µÄŹĒŃĒĻõĖįøłĄė×Ó | |
| C£® | BµÄpH£¼7 | |
| D£® | ¹ĢĢåÓÉBa£ØOH£©2”¢AlCl3”¢Na2SO3×é³É |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¾ŪĀČŅŅĻ©·Ö×ÓÖŠŗ¬Ģ¼Ģ¼Ė«¼ü | |
| B£® | ŅŌµķ·ŪĪŖŌĮĻæÉÖĘČ”ŅŅĖįŅŅõ„ | |
| C£® | °ü×°ÓĆ²ÄĮĻ¾ŪŅŅĻ©ŗĶ¾ŪĀČŅŅĻ©¶¼ŹōÓŚĢž | |
| D£® | ÓĶÖ¬µÄŌķ»Æ·“Ó¦ŹōÓŚ¼Ó³É·“Ó¦ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 5.6L | B£® | 6.72L | C£® | 2.8L | D£® | 13.44L |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
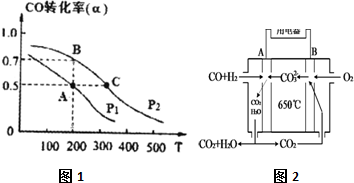
 £¬7.8gøĆ»ÆŗĻĪļÓė×ćĮæµÄCO2·“Ó¦£¬×ŖŅʵē×ÓŹżÄæĪŖ6.02”Į1022£¬¹ĢĢåŌöÖŲĪŖ2.8g£®
£¬7.8gøĆ»ÆŗĻĪļÓė×ćĮæµÄCO2·“Ó¦£¬×ŖŅʵē×ÓŹżÄæĪŖ6.02”Į1022£¬¹ĢĢåŌöÖŲĪŖ2.8g£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
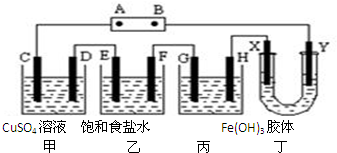 ½«ĻĀĮŠ×°ÖĆČēĶ¼Į¬½Ó£¬D”¢F”¢X”¢Y”¢E ¶¼ŹĒ²¬µē¼«£¬CŹĒĢśµē¼«£®¼×£¬ŅŅ£¬±ūČżøö×°ÖĆÖŠµē½āĒ°ŗóČÜŅŗµÄĢå»ż¶¼ŹĒ500mL£®½«µēŌ“½ÓĶØŗó£¬ĻņŅŅÖŠµĪČė·ÓĢŖŹŌŅŗ£¬ŌŚF¼«ø½½üĻŌŗģÉ«£®ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ£Ø””””£©
½«ĻĀĮŠ×°ÖĆČēĶ¼Į¬½Ó£¬D”¢F”¢X”¢Y”¢E ¶¼ŹĒ²¬µē¼«£¬CŹĒĢśµē¼«£®¼×£¬ŅŅ£¬±ūČżøö×°ÖĆÖŠµē½āĒ°ŗóČÜŅŗµÄĢå»ż¶¼ŹĒ500mL£®½«µēŌ“½ÓĶØŗó£¬ĻņŅŅÖŠµĪČė·ÓĢŖŹŌŅŗ£¬ŌŚF¼«ø½½üĻŌŗģÉ«£®ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ£Ø””””£©| A£® | µēŌ“B ¼«µÄĆū³ĘŹĒøŗ¼«£¬¶”ÖŠY¼«ø½½üŃÕÉ«±äÉī | |
| B£® | ŅŅ×°ÖĆÖŠµē½āŅ»¶ĪŹ±¼äŗ󣬼ÓČė0.2molŃĪĖįŌņæÉŅŌ»Öø“ŌĄ“µÄÅØ¶Č | |
| C£® | Éč¼×³ŲÖŠČÜŅŗµÄĢå»żŌŚµē½āĒ°ŗó¶¼ŹĒ500ml£¬µ±ŅŅ³ŲĖł²śÉśĘųĢåµÄĢå»żĪŖ4.48L£Ø±ź×¼×“æö£©Ź±£¬¼×³ŲÖŠĖłÉś³ÉĪļÖŹµÄĪļÖŹµÄĮæÅضČĪŖ0.2mol/L | |
| D£® | ¼××°ÖĆÖŠµē½ā·“Ó¦µÄ×Ü»Æѧ·½³ĢŹ½ŹĒ£ŗCuSO4+Fe$\frac{\underline{\;µē½ā\;}}{\;}$Cu+FeSO4 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŹµŃéŗóŹ£ÓąÉŁĮæÄĘæÉ·Å»ŲŌŹŌ¼ĮĘæÖŠ | |
| B£® | ÓĆŅ»°ćµÄ»Æѧ»¹Ō·Ø²»ÄÜÖĘČ”½šŹōÄĘ | |
| C£® | ijĪļÖŹµÄŃęÉ«·“Ó¦ĪŖ»ĘÉ«£¬ŌņøĆĪļÖŹŅ»¶Øŗ¬ÄĘŌŖĖŲ | |
| D£® | ÄĘæÉŅŌÓĆÉŁĮæĖ®ĆÜ·ā±£“ę |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com