
| A. | 它的元素符号为O | |
| B. | 它的核外电子排布式为1s22s22p63s23p4 | |
| C. | 可以与H2化合生成液态化合物 | |
| D. | 其电子排布图为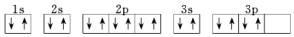 |
分析 价电子排布为3s23p4的粒子其基态原子核外电子排布式为1s22s22p63s23p4,其核外电子数为16,为S元素,据此分析解答.
解答 解:A.价电子排布为3s23p4的粒子,其基态原子核外电子排布式为1s22s22p63s23p4,其核外电子数为16,为S元素,故A错误;
B.价电子排布为3s23p4的粒子,其基态原子核外电子排布式为1s22s22p63s23p4,故B正确;
C.一定条件下,它可与H2生成气态化合物H2S,故C错误;
D.S原子核外电子排布遵循能量最低原理、保里不相容原理、洪特规则,其轨道表示式为 ,故D错误;
,故D错误;
故选B.
点评 本题考查了元素原子核外电子排布、元素的性质等知识点,难度不大,原子核外电子排布式或价电子排布式的书写是高考热点,要熟练掌握.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
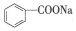 ,缩写为NaA)可用作饮料的防腐剂.研究表明苯甲酸(HA)的抑菌能力显著高于A-.已知25℃时,HA的Ka=6.25×10-5,H2CO3的Ka1=4.17×10-7,Ka2=4.90×10-11.在生产碳酸饮料的过程中,除了添加NaA外,还需加压充入CO2气体.下列说法正确的是(温度为25℃,不考虑饮料中其他成分)( )
,缩写为NaA)可用作饮料的防腐剂.研究表明苯甲酸(HA)的抑菌能力显著高于A-.已知25℃时,HA的Ka=6.25×10-5,H2CO3的Ka1=4.17×10-7,Ka2=4.90×10-11.在生产碳酸饮料的过程中,除了添加NaA外,还需加压充入CO2气体.下列说法正确的是(温度为25℃,不考虑饮料中其他成分)( )| A. | 相比于未充CO2的饮料,碳酸饮料的抑菌能力较低 | |
| B. | 提高CO2充气压力,饮料中c(A-)不变 | |
| C. | 当pH为5.0时,饮料中$\frac{c(HA)}{c({A}^{-})}$=0.16 | |
| D. | 碳酸饮料中各种粒子的浓度关系为:c(H+)=c(HCO${\;}_{3}^{-}$)+2c(CO${\;}_{3}^{2-}$)+c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
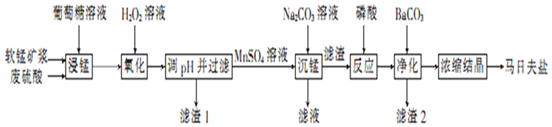
| 金属离子 | 开始沉淀的pH | 完全沉淀的pH |
| Fe3+ | 1.8 | 3.2 |
| Al3+ | 3.0 | 5.0 |
| Fe2+ | 5.8 | 8.8 |
| Mn2+ | 7.8 | 9.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氧化铝可作胃酸的中和剂 | B. | 工业上采用电解熔融氯化铝制铝 | ||
| C. | 铝罐可久盛食醋 | D. | 明矾用作净水剂不涉及化学变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 生成0.1NA根共价键 | B. | 消耗反应物总体积2.24L | ||
| C. | 转移了2NA个电子 | D. | 产物溶于水后,溶液pH=1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 大量塑料废弃物会造成严重的白色污染,应将其焚烧处理 | |
| B. | 应用放射性同位素发射出的射线,可进行食物保鲜和肿瘤治疗 | |
| C. | 过度开采使用煤、石油等化石燃料,会导致空气中PM2.5浓度升高 | |
| D. | 近两年全国普遍取消了各种节日焰火晚会,对减缓空气污染起到了一定作用 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com