
【题目】如图,图1表示白磷(P4)的分子结构,图2表示三氧化二磷(P4O6)的分子结构,图3表示五氧化二磷(P4O10)的分子结构,下列说法中正确的是( ) 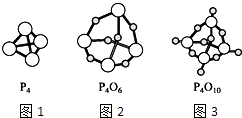
A.P4O6中的磷原子采用sp2方式杂化
B.三氧化二磷、五氧化二磷这两个名称都表示分子的实际组成
C.P4、P4O6和P4O10分子中同一P原子上两个化学键之间的夹角都是60°
D.P4O6分子中4个P原子构成正四面体,6个O原子构成正八面体
【答案】D
【解析】解:A.P4O6中的磷原子杂化轨道数=σ键数+孤对电子对数=3+1=4,所以采取sp3杂化;故A错误; B.三氧化二磷、五氧化二磷只表示原子个数比,这两个名称都未表示分子的实际组成,应为P4O6、P4O10 , 故B错误;
C.P4为正四面体结构,四个磷处在正四面体的顶点,同一P原子上两个化学键之间的夹角是60°,两个磷之间插入一个氧原子,得到P4O6 , P4O6四个磷再插入一个氧原子得到P4O10 , P4O6和P4O10分子中同一P原子上化学键之间的夹角近似等于109°28′,故C错误;
D.P4为正四面体结构,四个磷处在正四面体的顶点,两个磷之间插入一个氧原子,得到P4O6 , 在P4O6分子中,4个P原子构成正四面体,6个O原子构成正八面体,故D正确;
故选D.


科目:高中化学 来源: 题型:
【题目】一定温度下,向10 mL 0.40 mol·L-1 H2O2溶液中加入适量FeCl3溶液,不同时刻测得生成O2的体积(已折算为标准状况)如下表所示:
t / min | 0 | 2 | 4 | 6 |
V(O2) / mL | 0 | 9.9 | 17.2 | 22.4 |
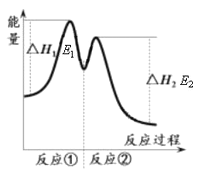
资料显示,反应分两步进行:① 2Fe3++H2O2 == 2Fe2++O2↑+2H+,② H2O2+2Fe2++2H+ == 2H2O+2Fe3+。反应过程中能量变化如下图所示。下列说法错误的是
A. Fe3+的作用是增大过氧化氢的分解速率
B. 反应①是吸热反应、反应②是放热反应
C. 反应2H2O2(aq) == 2H2O(l)+O2(g)的ΔH=E1-E2<0
D. 0~6 min的平均反应速率:v(H2O2)=3.33×10-2 mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关化学用语的使用正确的是( )
A.Cl2通入石灰乳中制漂白粉的离子方程式:Cl2+2OH﹣═Cl﹣+ClO﹣+H2O
B.利用泡沫灭火器灭火时发生的反应:2Al3++CO32﹣+3H2O═2Al(OH)3↓+CO2↑
C.已知离子的还原性:Sn2+>Fe2+ , 则可推测在溶液中能发生如下反应:Sn4++2Fe2+═2Fe3++Sn2+
D.298 K时,已知12g石墨完全燃烧生成CO2(g)放出393.5kJ热量,1mol CO完全燃烧放出283.5kJ热量,则一定有:C(s,石墨)+ ![]() O2(g)═CO(g)△H=﹣110 kJ?mol﹣1
O2(g)═CO(g)△H=﹣110 kJ?mol﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应2KMnO4+16HCl═2KCl+2MnCl2+5Cl2↑+8H2O中,还原剂与还原产物的物质的量之比为
A. 1:8 B. 8:1 C. 1:5 D. 5:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酰氯(SO2Cl2)是无色有刺激性气味的液体,熔点为-54.1℃,沸点为69℃,在潮湿空气中易“发烟”。实验室利用SO2(g)和Cl2(g)合成硫酰氯的实验装置如下图所示(部分夹持装置已省略):
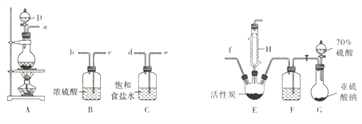
回答下列问题:
(1)实验室制备干燥纯净的氯气可以用A、B、C装置来完成,请连接装置接口:a→___,____→___,______→f(按气流流动方尚;用小写学母表示)。
(2)实验过程中,使用分液漏斗滴加浓硫酸的操作是_____________。
(3)装置C的作用是____________;装置B和F中浓硫酸起到的作用是①____________;②可观察到____________(填现象)来反映通入气体的速率,利用反应液滴加的快慢对气体通入速率加以控制,从而使通入反应器的SO2和Cl2达到最佳反应比例。
(4)该装置存在明显的缺陷,请指出:________________。
(5)已知该法合成硫酰氯为可逆反应,每生成2.7g硫酰氯放出热量1940J,写出该反应的热化学方程式: ________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
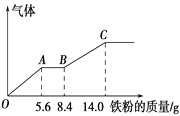
【题目】某稀硫酸和稀硝酸的混合溶液200 mL,平均分成两份。向其中一份中逐渐加入铜粉,最多能溶解9.6 g。向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如下图所示(已知硝酸只被还原为NO气体),下列分析或结果错误的是
A. 原混合酸中HNO3的物质的量为0.1 mol
B. OA段产生的是NO,AB段的反应为Fe+2Fe3+ == 3Fe2+,BC段产生氢气
C. 第二份溶液中最终溶质为FeSO4
D. H2SO4浓度为2.5 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,在体积为10 L的密闭容器中,1 mol X和1 mol Y进行反应:2X(g)+Y(g)![]() Z(g) △H<0,反应经60s达到平衡并生成0.3 mol Z,则下列说法中正确的是
Z(g) △H<0,反应经60s达到平衡并生成0.3 mol Z,则下列说法中正确的是
A. 以Y浓度变化表示的反应速率为0.0005 mol/(L·s)
B. 其他条件不变,将容器体积扩大至20 L,则Z的平衡浓度变为原来的1/2
C. 其他条件不变,将容器体积缩小至5L,平衡正向移动,平衡常数增大
D. 其他条件不变,升高温度逆反应速率加快,正反应速率减慢
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国有丰富的海水资源,开发和利用海水资源是当前科学研究的一项重要任务,下图是某化工厂对海水资源综合利用的示意图: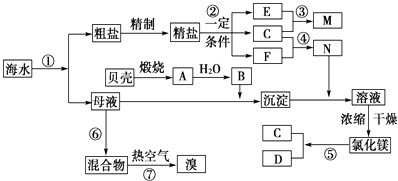
(1)Ⅰ.①写出N的化学式;②写出反应②的化学方程式 .
(2)Ⅱ.粗盐中含有Ca2+、Mg2+、SO42﹣等杂质,精制时所用的试剂为:①盐酸②氯化钡溶液③氢氧化钠溶液④碳酸钠溶液,以上试剂添加的顺序可以为 .
A.②③④①
B.③④②①
C.④③②①
D.③②④①
(3)Ⅲ.提取粗盐后剩余的海水(母液)中,可用来提取Mg和Br2 . ①若用来提取Mg,根据上述提取Mg的流程,没有涉及到的反应类型是 .
A.分解反应 B.化合反应C.置换反应 D.复分解反应
②若用来提取Br2 , 反应⑥所用的气态氧化剂的寻找货源的设想,其中合理的是 .
A.从外地购买 B.在当地新建生产厂
C.从本厂生产烧碱处循环 D.从本厂生产镁单质处循环
③母液用来提取Mg和Br2先后顺序,甲乙两位工程师有不同观点:
甲:母液先提取Mg,后提取Br2乙:母液先提取Br2 , 后提取Mg
请你判断哪个更合适?(填“甲”或“乙),理由是 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com