
| A. | 若容器内压强不再变化,则说明该反应己达平衡 | |
| B. | 反应前H2S物质的量为2.5mol | |
| C. | CO和H2S达平衡后的转化率相同 | |
| D. | 若平衡后再加入CO,则正反应速率增大,逆反应速率减小 |
分析 A.反应前后气体体积不变,反应过程中和平衡状态下压强始终不变;
B.反应前CO的物质的量为10mol,平衡后CO物质的量为8mol,转化的CO为2mol,设反应前H2S物质的量为nmol,表示出平衡时各物质的物质的量,由于反应前后气体物质的量不变,用物质的量代替浓度代入平衡常数K=$\frac{c(COS)c({H}_{2})}{c(CO)c({H}_{2}S)}$=0.1列方程计算解答;
C.依据B计算分析CO、H2S的转化率;
D.通入CO后瞬间正反应速率增大、逆反应速率不变,平衡正向移动,正反应速率减小、逆反应速率增大到新平衡时相等;
解答 解:A.CO (g)+H2S (g)?COS (g)+H2 (g),反应前后气体体积不变,反应过程中和平衡状态下压强始终不变,容器内压强不再变化,不能说明该反应己达平衡,故A错误;
B.反应前CO的物质的量为10mol,平衡后CO物质的量为8mol,转化的CO为2mol,设反应前H2S物质的量为nmol,则:
CO(g)+H2S(g)?COS(g)+H2(g)
起始(mol):10 n 0 0
变化(mol):2 2 2 2
平衡(mol):8 n-2 2 2
由于反应前后气体物质的量不变,用物质的量代替浓度计算平衡常数,则K=$\frac{c(COS)c({H}_{2})}{c(CO)c({H}_{2}S)}$=$\frac{2×2}{8×(n-2)}$=1,解得n=2.5,故B正确;
C.CO和H2S的起始量不同,反应消耗量相同,转化率一定不同,故C错误;
D.通入CO后瞬间正反应速率增大、逆反应速率不变,平衡正向移动,正反应速率减小、逆反应速率增大到新平衡时相等,故通入CO后重新达平衡,正、逆反应速率均增大,故D错误;
故选B.
点评 本题考查化学平衡计算、化学平衡建立,难度中等,注意三段式在化学平衡计算中应用,掌握基础是关键.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子数目相等的三种气体,质量最大的是Z | |
| B. | 相同条件下,同质量的三种气体,气体密度最小的是X | |
| C. | 若一定条件下,三种气体体积均为2.24L,则它们的物质的量一定均为0.1mol | |
| D. | 同温下,体积相同的两容器分别充2gY气体和1gZ气体,则其压强比为2:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 压强(Pa) | 4×105 | 6×105 | 10×105 | 20×105 |
| D的浓度(mol/L) | 0.085 | 0.126 | 0.200 | 0.440 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
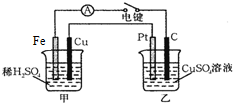 原电池和电解池都能实现能量的置换.回答下列问题:
原电池和电解池都能实现能量的置换.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙醇和乙醚互为同分异构体 | |
| B. | 干馏煤可以得到甲烷、苯和氨等重要化工原料 | |
| C. | 乙醇和乙酸之间能发生酯化反应,酯化反应和皂化反应互为逆反应 | |
| D. | 在酸性条件下,蔗糖水解的化学方程式为 C12H22O11+H2O→2C6H12O6(葡萄糖) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 气体W为氧气 | |
| B. | b极与电源的正极相连 | |
| C. | 离子交换膜c为阳离子交换膜 | |
| D. | a极的电极反应为SO2+2H2O-2e-=SO42-+4H+. |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com