
| A. | 用酸性KMnO4溶液鉴别CH3CH3和CH2=CH2 | |
| B. | 将盛有等体积CH4和Cl2的大试管倒扣在水槽中光照,试管内不能充满液体 | |
| C. | 用NaOH溶液除去乙酸乙酯中的少量乙酸 | |
| D. | 用NaOH溶液和新制Cu(OH)2悬浊液检验淀粉在稀H2SO4作用下是否水解 |
分析 A.乙烯能被高锰酸钾氧化,而乙烷不能;
B.发生取代反应生成的氯代烃不溶于水,且CH3Cl为气体;
C.乙酸、乙酸乙酯均与NaOH溶液反应;
D.淀粉水解生成葡萄糖,在碱性条件下检验葡萄糖.
解答 解:A.乙烯能被高锰酸钾氧化,而乙烷不能,现象不同,高锰酸钾可鉴别,故A正确;
B.发生取代反应生成的氯代烃不溶于水,且CH3Cl为气体,则试管内不能充满液体,故B正确;
C.乙酸、乙酸乙酯均与NaOH溶液反应,不能除杂,用饱和碳酸钠溶液除杂,故C错误;
D.淀粉水解生成葡萄糖,用NaOH溶液和新制Cu(OH)2悬浊液检验葡萄糖可知淀粉是否水解,故D正确;
故选C.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,注意有机物的鉴别、除杂及检验,侧重分析与应用能力的考查,题目难度不大.


科目:高中化学 来源: 题型:选择题
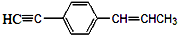
| A. | 所有碳原子不可能都在同一平面上 | |
| B. | 最多只可能有9个碳原子在同一平面上 | |
| C. | 有6个碳原子可能在同一直线上 | |
| D. | 只可能有5个碳原子在同一直线上 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2的燃烧热为241.8 kJ•mol-1 | |
| B. | 2H2(g)+O2(g)═2H2O(g)△H=-483.6 kJ•mol-1 | |
| C. | 1 mol H2完全燃烧生成液态水放出的热量大于241.8 kJ | |
| D. | 断开1 mol H2O的化学键吸收的总能量大于断裂1 mol H2和0.5 mol O2的化学键所吸收的总能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验操作 | 实验现象 | 实验结论 | |
| A | 向未知液中滴加氯水,再滴加KSCN溶液 | 溶液呈红色 | 未知液中一定含有Fe2+ |
| B | 向无色溶液中滴加氯水,再加CCl4振荡,静置 | 溶液分层,下层呈紫红色 | 无色溶液中一定含I- |
| C | 某气体通入品红溶液中 | 红色褪去 | 该气体中一定含SO2 |
| D | 将豆粒大金属钾投入水中 | 钾熔化成小球,在水面上游动 | 金属钾密度一定小于水 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ②③ | C. | ①④ | D. | ③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
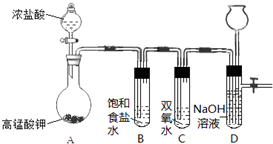 Cl2和H2O2是高中阶段最常见的两种氧化剂,经查阅资料Cl2氧化能力强于H2O2,能将H2O2氧化.为了验证某小组学生设计了如下图所示的实验装置进行实验(夹持装置略去).
Cl2和H2O2是高中阶段最常见的两种氧化剂,经查阅资料Cl2氧化能力强于H2O2,能将H2O2氧化.为了验证某小组学生设计了如下图所示的实验装置进行实验(夹持装置略去).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
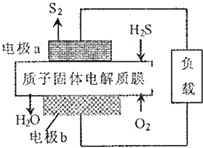 H2S利用是回收能最并得到单质硫.反应原理为:2H2S(g)+02(g)═S2(s)+2H20(1)△H=-632kJ•mol-1.下图为质子膜H2S燃料电池示意图.下列说法正确的是( )
H2S利用是回收能最并得到单质硫.反应原理为:2H2S(g)+02(g)═S2(s)+2H20(1)△H=-632kJ•mol-1.下图为质子膜H2S燃料电池示意图.下列说法正确的是( )| A. | 该电池可实现把化学能全部转化为电能 | |
| B. | 电极b上发生的电极反应为:02+2H2O+4e-═40H- | |
| C. | 电极a上发生的电极反应为:2H2S-4e-═S2+4H+ | |
| D. | 当有34gH2S参与反应时,有2mo1H+经质子膜进人负极区 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
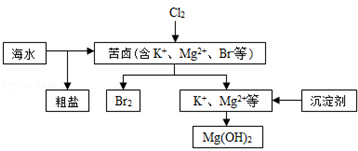
| A. | 向苦卤中通入Cl2是为了提取溴 | |
| B. | 粗盐可采用除杂、过滤、蒸发结晶等过程提纯 | |
| C. | 工业生产常选用NaOH作为沉淀剂 | |
| D. | 单质溴可用SO2将其还原吸收 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com