
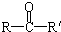 ��R��R����������Hԭ�ӣ��������Ϸ�Ӧ�����µ��л����ˮ��
��R��R����������Hԭ�ӣ��������Ϸ�Ӧ�����µ��л����ˮ��
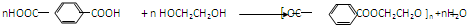
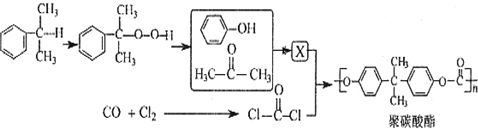
 ��Ӧ�ϳɾ�̼�����Ļ�ѧ����ʽ������д��Ӧ��������
��Ӧ�ϳɾ�̼�����Ļ�ѧ����ʽ������д��Ӧ��������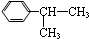 ��Ϊͬ���칹����л�����
��Ϊͬ���칹����л�����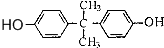 �������Ϸ��ǻ����ڻ����Hԭ���ܺ��巢��ȡ����Ӧ��
�������Ϸ��ǻ����ڻ����Hԭ���ܺ��巢��ȡ����Ӧ�� ��ClCOCl��һ�������·���ȡ����Ӧ����
��ClCOCl��һ�������·���ȡ����Ӧ����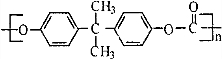 ���ݴ˽��1����2����3����
���ݴ˽��1����2����3����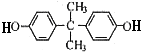 ��
�� ��
�� 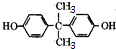 ��
��  �������۷�Ӧ���ɾ�̼��������Ӧ�Ļ�ѧ����ʽΪ��
�������۷�Ӧ���ɾ�̼��������Ӧ�Ļ�ѧ����ʽΪ��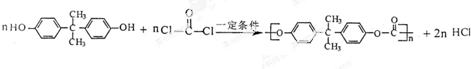 ��
�� ��
�� ��Ϊͬ���칹����л����У��ٲ�������1��ȡ����������������������ڲ�����������ȡ�����������һ��������ڡ��䡢��3�ֽṹ���۲�������3����ʱ�����ڵĽṹ�У�3�������ڡ����������ڡ�3�������ڼ�λ���ܹ���3�ֽṹ��������
��Ϊͬ���칹����л����У��ٲ�������1��ȡ����������������������ڲ�����������ȡ�����������һ��������ڡ��䡢��3�ֽṹ���۲�������3����ʱ�����ڵĽṹ�У�3�������ڡ����������ڡ�3�������ڼ�λ���ܹ���3�ֽṹ�������� ��Ϊͬϵ���ͬ���칹���ܹ��У�1+3+3=7�֣�
��Ϊͬϵ���ͬ���칹���ܹ��У�1+3+3=7�֣�


| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��2.3�˽����Ʊ�Ϊ������ʧȥ�ĵ�����ĿΪ0.1NA |
| B��18��ˮ�����еĵ�����ĿΪNA |
| C�����³�ѹ�£�11.2L����������ԭ����ĿΪNA |
| D��2.8��N2��CO��������ԭ����ĿΪ2NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��������SO2ͨ�뵽Ư����Һ�У�ClO-+SO2+H2O=HClO+HSO3- |
| B��Fe��OH��2��ϡ���ᷴӦ��2H++Fe��OH��2=Fe2++2H2O |
| C����NH4HCO3��Һ�м�������NaOH��Һ�����ȣ�HCO3-+NH4++2OH-=NH3��+2H2O+CO32- |
| D����ǿ����Һ�д���������Fe��OH��3��Ӧ����Na2FeO4��3ClO-+2Fe��OH��3=2FeO42-+3Cl-+H2O+4H+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����ά���¶Ȳ��䣬��ʼʱ����Ͷ��3mol A��1 mol B������Ͷ��3 mol A��l mol B��2mol C����ﵽƽ��ʱ����������B��ת���ʢ�=�� |
| B������ʼ�¶���ͬ���ֱ������������г���3 mol A��1mol B����ﵽƽ��ʱ��������C���ʵİٷֺ����ɴ�С��˳��Ϊ�ۣ��ڣ��� |
| C������ʼ�¶���ͬ���ֱ������������г���1 mol A��1molB��ﵽƽ��ʱ��������C���ʵİٷֺ���һ����ͬ |
| D������ʼ�¶���ͬ���ֱ������������г���3a mol A��a molB��ﵽƽ��ʱ��������A���ʵ�ת����һ����ͬ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����������ָ��������в�����Ԫ�ص��ᣬ��HCl��CH4�� |
| B�����ᷴӦ�����κ�ˮ������һ���Ǽ��������� |
| C�����е����������ﶼ������ˮ���ϵõ���Ӧ���� |
| D�������ܽ��ԵIJ�ͬ���ɽ����Ϊ�����Լ�Ϳ����Լ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
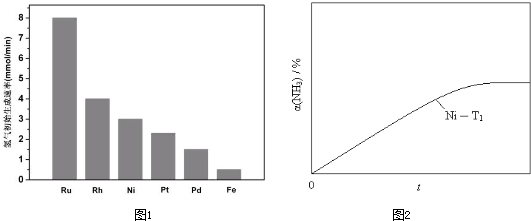
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A������������ˮ��Ӧ |
| B������������������Ӧ |
| C���ֱ����ȼ�� |
| D����һ��������ͨ������ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com