
【题目】下列离子方程式书写正确的是( )
A. 盐酸和氨水反应H++OH=H2O、B. 钠和冷水反应Na+2H2O=Na++2OH+H2↑
C. 氯气和氢氧化钠溶液反应Cl2+2OH=Cl+ClO+H2OD. 铜和稀硝酸反应Cu+2NO3+4H+=2Cu2++2NO2↑+2H2O
科目:高中化学 来源: 题型:
【题目】在容积为2 L的密闭容器中进行如下反应:
A(g)+2B(g)![]() 3C(g)+nD(g),开始时A为4 mol,B为6 mol;5 min末时测得C的物质的量为3 mol,用D表示的化学反应速率v(D)为0.2 mol·L-1·min-1。
3C(g)+nD(g),开始时A为4 mol,B为6 mol;5 min末时测得C的物质的量为3 mol,用D表示的化学反应速率v(D)为0.2 mol·L-1·min-1。
计算:
(1)5 min末A的物质的量浓度为____________________________________________。
(2)5 min内用B表示的化学反应速率v(B)为__________________________________。
(3)化学方程式中n值为___________________________________________________。
(4)此反应在四种不同情况下的反应速率分别为
①v(A)=5 mol·L-1·min-1
②v(B)=6 mol·L-1·min-1
③v(C)=4.5 mol·L-1·min-1
④v(D)=8 mol·L-1·min-1
其中反应速率最快的是______________(填编号)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁是生产生活中应用最广泛的一种金属。某化学学习小组在实验室中探究铁钉(主要成分为低碳钢)与热浓硫酸的反应。其探究流程如图所示:
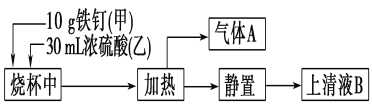
(1)从实验安全的角度考虑,应先向烧杯中加入______(填“甲”或“乙”);根据加入的反应物的量,实验需要选取的烧杯的规格为________(填字母序号)。
a.50 mL b.100 mL c.500 mL d.1 000 mL
(2)上清液B中可能既含Fe3+,又含Fe2+,要检验上清液B中有无Fe2+,应加入的试剂是________(填字母序号)。
a.KSCN溶液和氯水 b.铁粉和KSCN溶液
c.NaOH溶液 d.酸性KMnO4溶液
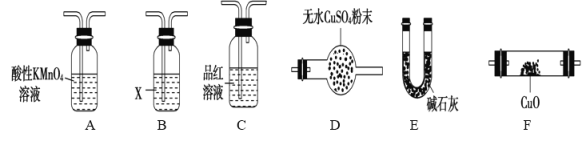
(3)气体A的主要成分是SO2,还可能含有H2和CO2。流程图中“加热”时可能生成CO2的原因是(用化学方程式表示)___________________。利用下列仪器可以同时检验气体A中是否含有H2和CO2(其中的夹持仪器、橡胶管和加热装置已经略去),则仪器的连接顺序是____________
(4)烧杯中的产物之一FeSO4有如下转化关系 (无关物质已略去)。
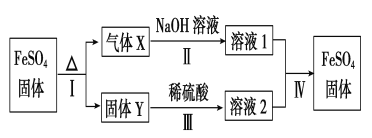
已知:①X由两种化合物组成,将X通入品红溶液,溶液褪色;通入BaCl2溶液,产生白色沉淀。②Y是红棕色的化合物。反应Ⅰ的化学方程式为_________________X通入BaCl2溶液,产生白色沉淀的化学式为________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)将金属钠置于空气中的加热,可以观察到有淡黄色固体生成,试写出该物质的电子式:___;如金属钠中混有少量金属钾,如何鉴别钾元素的存在?试简述实验操作及对应现象 ______________;
(2)在实验室模拟侯氏制碱法制备碳酸钠:一定温度下,往一定量饱和NaCl溶液中通入氨气达到饱和后,再不断通入CO2,一段时间后,出现沉淀,过滤得到NaHCO3晶体。该过程的化学方程式为:_____________。
(3)加热NaHCO3得到纯碱制品,实验室可进行此操作的装置可以是_____________。

(4)某实验小组通过下列实验探究过氧化钠与水的反应:

①用化学方程式解释使酚酞试液变红的原因_________,依据实验现象推测红色褪去的原因是_________。
②加入MnO2反应的化学方程式为_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酸钠(NaNO2)是一种重要的工业盐,易溶于水,微溶于乙醇。某化学兴趣小组对亚硝酸钠进行多角度探究:
Ⅰ.亚硝酸钠的制备。

(1)装置B的作用是___________________________________________。
(2)D中澄清石灰水变浑浊,则C中制备NaNO2的离子方程式为______________。
Ⅱ.探究亚硝酸钠与硫酸反应的气体产物成分。
已知:①NO+NO2+2OH-=2NO+H2O
②气体液化的温度:NO2为21 ℃,NO为-152 ℃
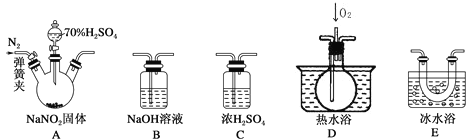
(3)反应前应打开弹簧夹,先通入一段时间氮气,目的是_______________________。
(4)仪器的连接顺序(按左→右连接):A→C→________。
(5)在关闭弹簧夹,打开分液漏斗活塞,滴入70%硫酸后,装置A中产生红棕色气体。
①确认装置A中产生的气体含有NO,依据的现象是_______________________。
②若D中通入过量O2,装置B中的化学方程式是_______________________。
Ⅲ.设计实验证明酸性条件下NaNO2具有氧化性。
(6)供选用的试剂:NaNO2溶液、KMnO4溶液、Fe2(SO4)3溶液、KI溶液、稀硫酸、淀粉溶液、KSCN溶液___________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学上常用燃烧法确定有机物的组成。下图装置是用燃烧法确定有机物化学式常用的装置,这种方法是在电炉加热时用纯氧氧化管内样品,根据产物的质量确定有机物的组成。
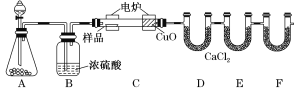
回答下列问题:
(1)A装置中盛放黑色固体分液漏斗盛放的物质是__________(名称)
(2)C装置(燃烧管)中CuO的作用是将有机物中的某元素充分氧化生成___________(化学式)
(3)写出E装置中所盛放试剂的名称__________,它的作用是吸收___________(化学式)。
(4)若将B装置去掉会使 __________(元素名称)元素的含量偏__________(大、小)
(5)若准确称取1.20 g样品(只含C、H、O三种元素中的两种或三种),经充分燃烧后,E管质量增加1.76 g,D管质量增加0.72 g,则该有机物的最简式为____________。
(6)要确定该有机物的化学式,还需要测定______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下溶液的酸碱性对TiO2光催化燃料R降解反应的影响如图所示。下列判断正确的是

A.溶液酸性越强,R 的降解速率越小
B.R的起始浓度越小,降解速率越大[
C.在0~50 min之间,pH=2和PH=7时R的降解百分率相等
D.在20~25 min之间,pH=10 时R的平均降解速率为0.04 mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在铁粉和过量2mol/L的稀H2SO4反应中,下列各措施能加快的速率,但又不影响H2的总量的是( )
A.加入少量的CuSO4溶液B.将2mol/L的稀硫酸改成98%的浓硫酸
C.将铁粉改为铁片D.加热
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com