
| A.pH为2的醋酸溶液与pH为12的氢氧化钠溶液 |
| B.0.01 mol·L-1的醋酸溶液与0.01 mol·L-1的氢氧化钠溶液 |
| C.pH为2的硫酸溶液与pH为12的氢氧化钠溶液 |
| D.0.01 mol·L-1的盐酸溶液与0.01 mol·L-1的氢氧化钡溶液 |
科目:高中化学 来源:不详 题型:单选题
| A.50 mL 1.5 mol·L-1的FeCl2溶液 | B.100 mL 3 mol·L-1的NH4Cl溶液 |
| C.75 mL 3 mol·L-1的KCl溶液 | D.50 mL 2 mol·L-1的CaCl2溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.滴定达终点时,俯视读数 |
| B.碱液移入锥形瓶后,加入10mL蒸馏水 |
| C.酸式滴定管用蒸馏水洗涤后,未用标准液润洗 |
| D.滴定振荡锥形瓶过程中,有少量溶液溅出 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.V(NaOH)=0时,c(H+)=1×10-2 mol/L |
| B.V(NaOH)=10 mL时,c(H+)=1×10-7 mol/L |
C.V(NaOH)<10 mL时,可能存在c(Na+)= |
D.V(NaOH)>10 mL时, > > > > ) ) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
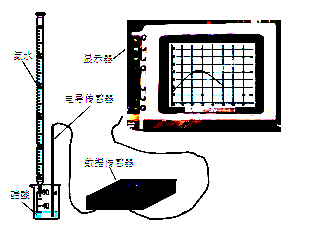
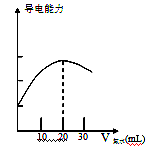
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.(NH4)2SO4溶液呈酸性是因为NH4+电离出H+ |
| B.因为醋酸是弱酸,所以醋酸促进了水的电离 |
| C.CH3COOH和(NH4)2SO4溶液中水电离出来的H+的物质的量浓度相等 |
| D.CH3COOH和(NH4)2SO4两水溶液呈酸性的原因不同 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.原混合气体中氮气与二氧化碳体积之比为1∶4 |
| B.在逐滴加入稀盐酸产生二氧化碳之前,发生的离子反应为CO32-+H-==HCO3- |
| C.溶 液 A 中 含 有 0 . 01 mol NaOH 和0.01 mol Na2CO3 |
| D.当加入0.1 L稀盐酸时,此时溶液中离子浓度大小关系为c(Na+)>c(Cl-)=c(CO32-)>c(OH-)>c(H+) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.盛装标准液的滴定管未用标准液润洗 |
| B.滴定终点读数时,仰视滴定管的刻度,其他操作正确 |
| C.盛装未知液的锥形瓶用蒸馏水洗过后再用未知液润洗 |
| D.滴定前无气泡,滴定到终点时,发现尖嘴处有气泡 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com