
在相同条件下,分别将下列气体等体积混合于四支大小相同的试管中:①NO与NO2;②NO与O2;③NO2与O2;④SO2与NO2,将四支试管倒立于水中,各试管中水面上升高度应为( )
A. ①>②>③>④ B. ②>③>④>① C. ①=②=③=④ D. ③>②>①>④
考点: 化学方程式的有关计算.
分析: 发生反应:①3NO2+H2O=2HNO3+NO,②4NO+3O2+2H2O=4HNO3,③4NO2+O2+2H2O=4HNO3,④NO2+SO2+H2O=NO+H2SO4,根据方程式判断水面上升高度.
解答: 解:①3NO2+H2O=2HNO3+NO,水面上升高度为试管的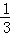 ;
;
②4NO+3O2+2H2O=4HNO3,水面上升高度为试管的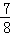 ;
;
③4NO2+O2+2H2O=4HNO3,水面上升高度为试管的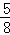 ;
;
④NO2+SO2+H2O=NO+H2SO4,水面上升高度为试管的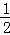 ,
,
故各试管水面上升高度应为②>③>④>①,
故选:B.
点评: 本题考查化学方程式有关计算,难度不大,明确发生的反应即可解答,注意利用总反应方程式解答.


科目:高中化学 来源: 题型:
下列说法正确的是()
A. HClO中氯元素化合价比HClO4中氯元素化合价低,所以HClO4的氧化性强
B. 已知①Fe+Cu2+═Fe2++Cu;②2Fe3++Cu═2Fe2++Cu2+,则氧化性强弱顺序为:Fe3+>Cu2+>Fe2+
C. 已知还原性:B﹣>C﹣>D﹣,反应 2C﹣+D2═2D﹣+C2和反应2C﹣+B2═2B﹣+C2都能发生
D. 具有强氧化性和强还原性的物质放在一起就能发生氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于实验现象的描述不正确的是()
A. 把铜片和铁片紧靠在一起浸入稀硫酸中,铜片表面出现气泡
B. 用锌片做阳极,铁片做阴极,电解氯化锌溶液,铁片表面出现一层锌
C. 把铜片插入三氯化铁溶液中,在铜片表面出现一层铁
D. 把锌粒放入盛有盐酸的试管中,加入几滴氯化铜溶液,气泡放出速率加快
查看答案和解析>>
科目:高中化学 来源: 题型:
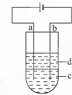
由于Fe(OH)2极易被氧化,所以实验室很难用亚铁盐溶液与烧碱反应制得白色纯净的Fe(OH)2沉淀.应用如下图所示电解实验可制得白色纯净的Fe(OH)2沉淀.两电极的材料分别为石墨和铁.
(1)a电极材料应为 ,电极反应式 ;
(2)电解液c可以是(填编号)
A.纯水 B.NaCl溶液 C.NaOH溶液 D.CuCl2溶液
(3)d为苯,其作用为 ,在加入苯之前对c应作怎样的简单处理? .
(4)为了在较短时间内看到白色沉淀,可采取的措施(填编号)
A.改用稀硫酸作电解液
B.适当增大电源的电压
C.适当减少两电极间距离
D.适当降低电解液的温度
(5)若c为Na2SO4溶液,当电解一段时间看到白色Fe(OH)2沉淀后,再反接电源电解,除了电极上看到气泡外,混合物中另一明显现象为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
已知KNO3晶体溶解于水时要吸收热量,从溶液中析出KNO3晶体时会放出热量.若有室温下KNO3饱和溶液20mL,向其中加入1g KNO3晶体,充分搅拌后,下列判断正确的是( )
A. 溶液质量增加 B. 溶液的温度降低
C. 晶体不再溶解 D. 溶液的温度和质量都不变
查看答案和解析>>
科目:高中化学 来源: 题型:
镭是元素周期表中第七周期第ⅡA族元素,关于其叙述不正确的是( )
A. 镭的金属性比钙弱 B. 单质能与水反应生成H2
C. 在化合物中呈+2价 D. 碳酸镭难溶于水
查看答案和解析>>
科目:高中化学 来源: 题型:
如图所示是298K时,N2与H2反应过程中能量变化的曲线图,下列叙述正确的是()
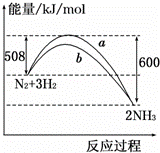
A. 该反应的热化学方程式为:N2+3H2⇌2NH3△H=﹣92 kJ/mol
B. a曲线是加入催化剂时的能量变化曲线
C. 加入催化剂,该化学反应的反应热改变
D. 在温度、体积一定的条件下,若通入2 mol N2和6 mol H2反应后放出的热量为Q kJ,则184>Q
查看答案和解析>>
科目:高中化学 来源: 题型:
2﹣丁炔与1,3﹣丁二烯分别跟氢气反应的热化学方程式如下:
CH3﹣C≡C﹣CH3(g)+2H2(g)→CH3CH2CH2CH3(g)+Q1
CH2=CH﹣CH=CH2(g)+2H2(g)→CH3CH2CH2CH3(g)+Q2
已知:Q1>Q2(Q1和Q2均大于零),由此不能判断()
A. 2﹣丁炔与1,3﹣丁二烯稳定性的相对大小
B. 2﹣丁炔与1,3﹣丁二烯分子储存能量的相对高低
C. 2﹣丁炔与1,3﹣丁二烯相互转化的热效应
D. 一个碳碳叁键的键能与两个碳碳双键的键能之和的大小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com