
下列各选项中对应的实验操作、现象和结论均正确的是
选项 | 实验操作 | 现 象 | 结 论 |
A | 在试管中滴入适量C2H5X与NaOH溶液,振荡、加热、静置分层后,取水层加稀硝酸酸化,再滴加数滴AgNO3溶液 | 淡黄色沉淀 | 证明卤代烃中含有溴元素 |
B | 将蘸有浓氨水的玻璃棒置于某无机酸浓溶液的试剂瓶口 | 有大量白烟 | 该无机酸一定为盐酸 |
C | 在大试管中依次加入适量丁醇、过量乙酸、几滴浓硫酸,混合后塞上带长导管的试管塞,放在石棉网上方空气中加热至120℃左右 | 反应液沸腾,冷却静置,上层油状透明液体有水果香味 | 该油状液体为乙酸丁酯 |
D | 在简易启普发生器中向石灰石中加入浓醋酸,将产生的气体直接通入苯酚钠溶液中 | 苯酚钠溶液产生浑浊 | 酸性:醋酸>碳酸>苯酚 |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:2014-2015学年天津市七校高三4月联考化学试卷(解析版) 题型:推断题
(共17分)各物质之间的转化关系如下图,部分生成物省略。C、D是由X、Y、Z中两种元素组成的化合物,X、Y、Z的原子序数依次增大,在周期表中X的原子半径最小,Y、Z原子最外层电子数之和为10。D为无色非可燃性气体,G为黄绿色单质气体,J、M为金属,I有漂白作用,反应①常用于制作印刷线路板。

请回答下列问题:
(1)G元素在周期表中的位置_________________,C的电子式____________________。
(2)比较Y与Z的原子半径大小______>______(填写元素符号)。
(3)写出E和乙醛反应的化学反应方程式(有机物用结构简式表示) ;反应类型: 。
(4)写出实验室制备G的离子反应方程式 。
(5)气体D与NaOH溶液反应可生成两种盐P和Q,在P中Na的质量分数为43%,其俗名为 。
(6)实验室中检验L溶液中的阳离子常选用 溶液,现象是 。
(7)A中包含X、Y、Z元素,A的化学式为 。
(8)研究表明:气体D在一定条件下可被还原为晶莹透明的晶体N,其结构中原子的排列为正四面体,请写出N及其1种同素异形体的名称______________、____________。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年四川省绵阳市高三第三次诊断性考试理综化学试卷(解析版) 题型:选择题
已知反应X(g)+Y(g) R(g)+Q(g)的平衡常数与温度的关系如下表。830℃时,向一个2 L的密闭容器中充入0.2 mol X和0.8 mol Y,反应初始4 s内
R(g)+Q(g)的平衡常数与温度的关系如下表。830℃时,向一个2 L的密闭容器中充入0.2 mol X和0.8 mol Y,反应初始4 s内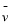 (X)=0.005 mol/(L·s)。下列说法正确的是
(X)=0.005 mol/(L·s)。下列说法正确的是
温度/℃ | 700 | 800 | 830 | 1000 | 1200 |
平衡常数 | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
A.4 s时容器内c(Y)=0.76 mol/L
B.830℃达平衡时,X的转化率为80%
C.反应达平衡后,升高温度,平衡正向移动
D.1200℃时反应R(g)+Q(g) X(g)+Y(g)的平衡常数K=0.4
X(g)+Y(g)的平衡常数K=0.4
查看答案和解析>>
科目:高中化学 来源:2014-2015学年四川省达州市第二次诊断性测试化学试卷(解析版) 题型:选择题
化学与生产生活社会密切相关下列说法中正确的是
A.食醋可用于除去暖水瓶中的水垢
B.14C可用于文物的年代鉴定,14C与12C互为同素异形体
C.淀粉纤维素和油脂都属于天然高分子化合物
D.pH在5.6~7.0之间的降水通常称为酸雨
查看答案和解析>>
科目:高中化学 来源:2014-2015学年上海市闵行区高三下学期质量调研考试(二模)化学试卷(解析版) 题型:填空题
(本题共12分)TiCl4是一种重要的化工原料,其工业生产过程如下:
2FeTiO3(s) + 7Cl2(g) + 6C (s) 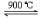 2TiCl4 (g) + 2FeCl3(g) + 6CO(g) – Q (Q>0)
2TiCl4 (g) + 2FeCl3(g) + 6CO(g) – Q (Q>0)
回答下列问题:
1.该反应达到平衡后,若使正反应速率增大可采取的方法有_________。(选填编号)
a.加压 b.加入碳 c.升温 d.及时移走CO
2.若上述反应在固定体积的密闭容器中发生,一定能说明反应已达平衡的是_______。(选填编号)
a. 反应物不再转化为生成物
b. 炉内FeTiO3与TiCl4 的质量比保持不变
c. 反应的热效应不再改变
d. 单位时间内,n(FeTiO3)消耗:n(FeCl3)生成=1:1
3.上述反应中所有非金属元素原子的半径从大到小的顺序为_____________;其中不属于同周期又不属于相邻族的两元素形成_____分子(填“极性”或“非极性”),通过比较____________可以判断这两种元素的非金属性。
4.上述反应中,非金属性最弱的元素原子的电子共占据_______个原子轨道,最外层电子排布式为____________。它形成的固态单质中只含一种强烈的相互作用力,则该单质属于______晶体。
5.为方便获得氯气,工业制TiCl4厂可以和氯碱厂进行联合生产。CO可合成甲醇,若不考虑损失,上述联合生产在充分利用各种副产品的前提下,合成192 kg甲醇,至少需补充H2 mol。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年上海市闵行区高三下学期质量调研考试(二模)化学试卷(解析版) 题型:选择题
在催化剂、400℃时可实现氯的循环利用,下图是其能量关系图,下列分析正确的是
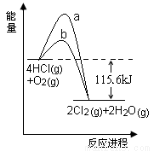
A.曲线a是使用了催化剂的能量变化曲线
B.反应物的总键能高于生成物的总键能
C.反应的热化学方程式为:4HCl(g) + O2(g) 2Cl2+2H2O(g)-115.6 kJ
2Cl2+2H2O(g)-115.6 kJ
D.若反应生成2mol液态水,放出的热量高于115.6kJ
查看答案和解析>>
科目:高中化学 来源:2014-2015学年上海市闵行区高三下学期质量调研考试(二模)化学试卷(解析版) 题型:选择题
下列事实能用元素周期律解释的是
A.沸点:H2O>H2Se>H2S B.酸性:H2SO4>H2CO3>HClO
C.硬度:I2>Br2>Cl2 D.碱性:KOH>NaOH>Al(OH)3
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江西省鹰潭市高三第二次模拟考试理综化学试卷(解析版) 题型:选择题
某无色稀溶液X中,可能含有下表所列离子中的某几种
阴离子 | CO32-、SiO32-、AlO2-、Cl- |
阳离子 | Al3+、Fe3+、Mg2+、NH4+、Na+ |
现取该溶液适量,向其中加入某试剂Y,产生沉淀的物质的量(n)与加入试剂Y体积(V)的关系如图所示,下列说话正确的是
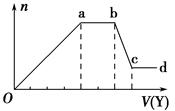
A.若Y是盐酸,则Oa段转化为沉淀的离子(上表中,下同)只有AlO2-
B.若Y是盐酸,则溶液中可能含有的阳离子是Al3+。
C.若Y是NaOH溶液,则bc段反应的离子方程式为 Al(OH)3+OH-=AlO2-+2H2O
D.若Y是NaOH溶液,则X溶液中只存四种离子是:Al3+、Fe3+ 、NH4+ 、Cl-
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖南省怀化市高三学业水平模拟考试化学试卷(解析版) 题型:选择题
下列实验方法能达到实验目的的是
A.用淀粉溶液检验溶液中是否存在碘单质
B.用分液漏斗分离水与乙醇的混合物
C.用氯化钡溶液鉴别碳酸钠溶液与硫酸钠溶液
D.用排水集气法收集氨气
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com