
| A.CH4 | B.CH2=CH2 | C.SO2 | D.HI |
科目:高中化学 来源:不详 题型:单选题
| A.NO | B.N2O | C.N2 | D.N2O3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.金属单质在反应中只作还原剂 |
| B.非金属单质在反应中只作氧化剂 |
| C.金属失电子越多,其还原性越强有力 |
| D.Cu2+比Fe2+氧化性强,Fe比Cu还原性强 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Cl2 | B.KMnO4 | C.HCl | D.FeCl3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.A原子的最外层电子数比B原子的最外层电子数少 |
| B.A原子的电子层数比B原子的电子层数多 |
| C.1mol A从酸中置换H+生成的H2比1mol B从酸中置换H+生成的H2多 |
| D.常温时,A能从水中置换出氢,而B不能 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.当x ≤ 时,反应的离子方程式为:2Fe2++ Cl2 → 2Fe3++ 2Cl- 时,反应的离子方程式为:2Fe2++ Cl2 → 2Fe3++ 2Cl- |
| B.当x ≥ n时,反应的离子方程式为:2Fe2++ 2I-+ 2Cl2 → 2Fe3++ I2+ 4Cl- |
| C.当Fe2+和I-同时被氧化时,x与n的关系为x>n |
| D.当x=n时,反应后氧化产物的物质的量为n mol |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
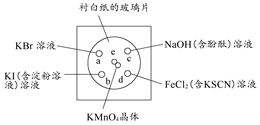
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com